Лечебно-профилактические препараты бактериофагов: эффективность, безопасность, международный опыт регулирования (обзор)
https://doi.org/10.30895/2312-7821-2026-14-1-90-100
Резюме
ВВЕДЕНИЕ. Препараты бактериофагов эффективны при бактериальных инфекциях, в том числе вызванных возбудителями с множественной лекарственной устойчивостью. Для разработки и широкого использования стандартизованных и персонализированных препаратов для фаготерапии необходима актуализация нормативных правовых и методических документов, регламентирующих разработку, проведение клинических исследований, регистрацию и обращение препаратов бактериофагов.
ЦЕЛЬ. Анализ мировых тенденций в области разработки, регистрации, оценки эффективности и безопасности препаратов бактериофагов для определения перспективных направлений развития фаготерапии в Российской Федерации.
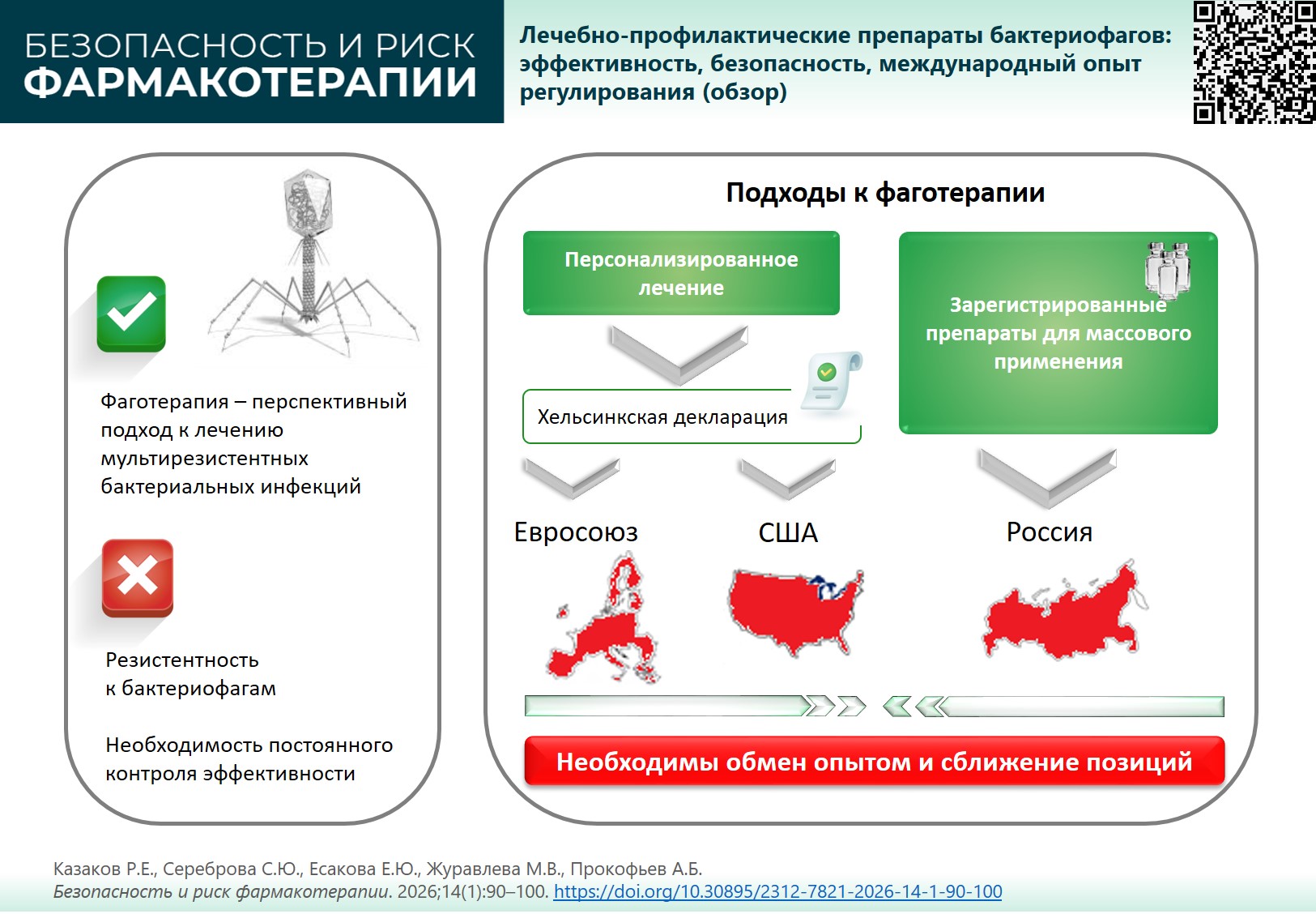
ОБСУЖДЕНИЕ. Несмотря на доказанную эффективность бактериофагов, их широкое внедрение в клиническую практику затрудняют быстрое развитие резистентности у возбудителей инфекций, сложности доставки к очагу инфекции, а также недостаточная изученность безопасности фаготерапии. При снижении эффективности стандартизованных препаратов бактериофагов может потребоваться изменение рецептуры для актуализации штаммов, однако регуляторные механизмы для этого отсутствуют. В Российской Федерации зарегистрированы и применяются 14 стандартизованных препаратов бактериофагов, проведены их клинические исследования. В меньшей степени развито персонализированное применение бактериофагов. В США и государствах – членах Европейского союза, предъявляющих строгие требования к доказательствам безопасности и эффективности лекарственной терапии, фаготерапия не является официальным методом лечения и применяется лишь в отдельных случаях. В некоторых европейских странах, в частности, в Польше и Бельгии, фаготерапии уделяется большое внимание, но применение бактериофагов остается индивидуальным. В 2025 г. в Европейском союзе подготовлена рабочая версия концептуального документа по разработке и производству препаратов на основе бактериофагов для применения у человека. Но до сих пор ни один препарат для фаговой терапии не получил одобрения в соответствии с законодательствами Европейского союза и США.
ВЫВОДЫ. Россия имеет уникальный опыт применения стандартизованных фаговых препаратов. При этом регуляторные механизмы внесения изменений в состав уже зарегистрированных препаратов бактериофагов не разработаны ни в России, ни в других странах. Для глобального развития направления необходима международная гармонизация нормативной базы с учетом новых инициатив Европейского союза и США по созданию регуляторных документов, а также интенсификация исследований по преодолению резистентности бактерий к бактериофагам и изучение их долгосрочной безопасности.
Ключевые слова
Об авторах
Р. Е. КазаковРоссия
Казаков Руслан Евгеньевич, канд. биол. наук
Петровский б-р, д. 8, стр. 2, Москва, 127051
С. Ю. Сереброва
Россия
Сереброва Светлана Юрьевна, д-р мед. наук, профессор
Петровский б-р, д. 8, стр. 2, Москва, 127051;
Трубецкая ул., д. 8, стр. 2, Москва, 119991
Е. Ю. Есакова
Россия
Есакова Елена Юрьевна, канд. фарм. наук
Петровский б-р, д. 8, стр. 2, Москва, 127051;
Трубецкая ул., д. 8, стр. 2, Москва, 119991
М. В. Журавлева
Россия
Журавлева Марина Владимировна, д-р мед. наук, профессор
Петровский б-р, д. 8, стр. 2, Москва, 127051;
Трубецкая ул., д. 8, стр. 2, Москва, 119991
А. Б. Прокофьев
Россия
Прокофьев Алексей Борисович, д-р мед. наук, профессор
Петровский б-р, д. 8, стр. 2, Москва, 127051;
Трубецкая ул., д. 8, стр. 2, Москва, 119991
Список литературы
1. Żaczek M, Weber-Dąbrowska B, Międzybrodzki R, et al. Phage therapy in Poland — a centennial journey to the first ethically approved treatment facility in Europe. Front Microbiol. 2020;11:1056. https://doi.org/10.3389/fmicb.2020.01056
2. Faltus T. The medicinal phage-regulatory roadmap for phage therapy under EU pharmaceutical legislation. Viruses. 2024;16(3):443. https://doi.org/10.3390/v16030443
3. Verbeken G, Pirnay JP, Lavigne R, et al. Viruses that can cure, when antibiotics fail. J Microb Biochem Technol. 2016;(8):21–4. https://doi.org/10.4172/1948-5948.1000257
4. Pirnay JP, Verbeken G, Ceyssens PJ, et al. The magistral phage. Viruses. 2018;10(2):64. https://doi.org/10.3390/v10020064
5. Pirnay JP, Verbeken G. Magistral phage preparations: Is this the model for everyone? Clin Infect Dis. 2023;77(Suppl 5):S360–9. https://doi.org/10.1093/cid/ciad481
6. Gordillo Altamirano FL, Barr JJ. Phage therapy in the postantibiotic era. Clin Microbiol Rev. 2019;32(2):e00066-18. https://doi.org/10.1128/CMR.00066-18
7. Pendleton JN, Gorman SP, Gilmore BF. Clinical relevance of the ¬ESKAPE pathogens. Expert Rev Anti Infect Ther. 2013;11(3):297–308. https://doi.org/10.1586/eri.13.12
8. Strathdee SA, Hatfull GF, Mutalik VK, Schooley RT. Phage therapy: From biological mechanisms to future directions. Cell. 2023;186(1):17–31. https://doi.org/10.1016/j.cell.2022.11.017
9. Debarbieux L, Pirnay JP, Verbeken G, et al. A bacteriophage journey at the European Medicines Agency. FEMS Microbiol Lett. 2016;363(2):fnv225. https://doi.org/10.1093/femsle/fnv225
10. Abdelkader K, Gerstmans H, Saafan A, et al. The preclinical and clinical progress of bacteriophages and their lytic enzymes: The parts are easier than the whole. Viruses. 2019;11(2):96. https://doi.org/10.3390/v11020096
11. Давыдов ДС, Парфенюк РЛ, Дурманова ЗВ и др. Особенности регулирования обращения лекарственных препаратов бактериофагов: международный опыт и перспективы развития. БИОпрепараты. Профилактика, диагностика, лечение. 2024;24(3):322–34. https://doi.org/10.30895/2221-996X-2024-24-3-322-334
12. Давыдов ДС, Парфенюк РЛ, Дурманова ЗВ и др. Особенности государственной регистрации и обеспечения качества лекарственных препаратов бактериофагов в Российской Федерации. БИОпрепараты. Профилактика, диагностика, лечение. 2023;23(2):181–93. https://doi.org/10.30895/2221-996X-2023-431
13. Kim MS, Kim YD, Hong SS, et al. Phage-encoded colanic acid-degrading enzyme permits lytic phage infection of a capsule-forming resistant mutant Escherichia coli strain. Appl Environ Microbiol. 2015;81(3):900–9. https://doi.org/10.1128/AEM.02606-14
14. Pires DP, Cleto S, Sillankorva S, et al. Genetically engineered phages: A review of advances over the last decade. Microbiol Mol Biol Rev. 2016;80(3):523–43. https://doi.org/10.1128/mmbr.00069-15
15. Ghatbale P, Blanc A, Sue A, et al. Experimental phage evolution results in expanded host ranges against antibiotic resistant Klebsiella pneumoniae isolates. Nat Commun. 2025;16(1):9903. https://doi.org/10.1038/s41467-025-66062-7
16. Gu Liu C, Green SI, Min L, et al. Phage-antibiotic synergy is driven by a unique combination of antibacterial mechanism of action and stoichiometry. mBio. 2020;11(4):e01462-20. https://doi.org/10.1128/mBio.01462-20
17. Malika DJ, Sokolova IJ, Vinnera GK, et al. Formulation, stabilisation and encapsulation of bacteriophage for phage therapy. Adv Colloid Interface Sci. 2017;249:100–33. https://doi.org/10.1016/j.cis.2017.05.014
18. Jault P, Leclerc T, Jennes S, et al. Efficacy and tolerability of a cocktail of bacteriophages to treat burn wounds infected by Pseudomonas aeruginosa (PhagoBurn): A randomised, controlled, double-blind phase 1/2 trial. Lancet. 2019;19(1):35–45. https://doi.org/10.1016/S1473-3099(18)30482-1
19. Huang G, Wei Z, Wang D. What do we lean from the “PhagoBurn” project. Burns. 2019;45(1):260. https://doi.org/10.1016/j.burns.2018.11.008
20. Бахрушина ЕО, Анурова МН, Алешкин АВ и др. Современные тенденции применения и создания лекарственных препаратов бактериофагов. Вестник Российской академии медицинских наук. 2021;76(4):351–60. https://doi.org/10.15690/vramn1380
21. Górski A, Międzybrodzki R, Węgrzyn G, et al. Phage therapy: Current status and perspectives. Med Res Rev. 2020;40(1):459–63. https://doi.org/10.1002/med.21593
22. Liu D, Van Belleghem JD, de Vries CR, et al. The safety and toxicity of phage therapy: A review of animal and clinical studies. Viruses. 2021;13(7):1268. https://doi.org/10.3390/v13071268
23. Steele A, Stacey HJ, de Soir S, Jones JD. The safety and efficacy of phage therapy for superficial bacterial infections: A systematic review. Antibiotics (Basel). 2020;9(11):754. https://doi.org/10.3390/antibiotics9110754
24. Verbeken G, Pimay JP, Lavigne R, et al. Call for a dedicated european legal framework for bacteriophage therapy. Arch Immunol Ther Exp (Warsz). 2014;62(2):117–29. https://doi.org/10.1007/s00005-014-0269-y
25. Wu N, Chen LK, Zhu T. Phage therapy for secondary bacterial infections with COVID-19. Curr Opin Virol. 2022;52:9–14. https://doi.org/10.1016/j.coviro.2021.11.001
26. Fukaya-Shiba A, Ogata A, Kuribayashi R, et al. Regulatory considerations for developing phage therapy medicinal products for the treatment of antimicrobial resistant bacterial infections. Front Pharmacol. 2025;16:1713471. https://doi.org/10.3389/fphar.2025.1713471
27. Kasurinen J, Spruit CM, Wicklund A, et al. Screening of bacteriophage encoded toxic proteins with a next generation sequencing-based assay. Viruses. 2021;13(5):750. https://doi.org/10.3390/v13050750
28. Uyttebroek S, Chen B, Onsea J, et al. Safety and efficacy of phage therapy in difficult-to-treat infections: a systematic review. Lancet Infect Dis. 2022;22(8):e208–20. https://doi.org/10.1016/s1473-3099(21)00612-5
29. Abedon ST, Thomas-Abedon C. Phage therapy pharmacology. Curr Pharm Biotechnol. 2010;11(1):28–47. https://doi.org/10.2174/138920110790725410
30. Loh B, Gondil VS, Manohar P, et al. Encapsulation and delivery of therapeutic phages. Appl Environ Microbiol. 2021;87(5):e01979–20. https://doi.org/10.1128/aem.01979-20
31. Karn SL, Gangwar M, Kumar R, et al. Phage therapy:A revolutionary shift in the management of bacterial infections, pioneering new horizons in clinical practice, and reimagining the arsenal against microbial pathogens. Front Med. 2023;10:1209782. https://doi.org/10.3389/fmed.2023.1209782
32. Bretaudeau L, Tremblais K, Aubrit F, et al. Good Manufacturing Practice (GMP) compliance for phage therapy medicinal products. Front Microbiol. 2020;11:1161. https://doi.org/10.3389/fmicb.2020.01161
33. Gorski A, Miedzybrodzki R, Weber-Dabrowska B, et al. Phage therapy: Combating infections with potential for evolving from merely a treatment for complications to targeting diseases. Front Microbiol. 2016;7:1515. https://doi.org/10.3389/fmicb.2016.01515
34. Dvořáčková M, Růžička F, Benešík M, et al. Antimicrobial effect of commercial phage preparation Stafal® on biofilm and planktonic forms of methicillin-resistant Staphylococcus aureus. Folia Microbiol (Praha). 2019;64(1):121–6. https://doi.org/10.1007/s12223-018-0622-3
35. Miedzybrodzki R, Fortuna W, Weber-Dabrowska B, Górski A. Phage therapy of staphylococcal infections (including MRSA) may be less expensive than antibiotic treatment. Postepy Hig Med Dosw (Online). 2007;61:461–5. PMID: 17679835
36. Романовский ГБ, Романовская ЕА, Дасаева АИ. Публично-правовое регулирование в сфере биомедицины в республике Польша. Актуальные проблемы государства и права. 2025;9(2):226–35. https://doi.org/10.20310/2587-9340-2025-9-2-226-235
37. Zaczek, M, Górski A, Weber-Dabrowska B, et al. Thorough synthesis of phage therapy unit activity in Poland — Its history, milestones and international recognition. Viruses. 2022;14:1170. https://doi.org/10.3390/v14061170
38. Eskenazi A, Lood C, Wubbolts J, et al. Combination of pre-adapted bacteriophage therapy and antibiotics for treatment of fracture-¬related infection due to pandrug-resistant Klebsiella pneumonia. Nat Commun. 2022;13(1):302. https://doi.org/10.1038/s41467-021-27656-z
39. Farrell AT, Goldberg KB, Pazdur R. Flexibility and innovation in the FDA’s novel regulatory approval strategies for hematologic drug. Blood. 2017;130(11):1285–9. https://doi.org/10.1182/blood-2017-04-742726
40. Ландышев НН, Воронько ЯГ, Тимошина ОЮ и др. Обзор законодательства в области обращения персонализированных препаратов бактериофагов. Вопросы вирусологии. 2020;65(5):259–66. https://doi.org/10.36233/0507-4088-2020-65-5-2
41. Voelker R. FDA approves bacteriophage trial. JAMA. 2019;321(7):638. https://doi.org/10.1001/jama.2019.0510
Рецензия
Для цитирования:
Казаков Р.Е., Сереброва С.Ю., Есакова Е.Ю., Журавлева М.В., Прокофьев А.Б. Лечебно-профилактические препараты бактериофагов: эффективность, безопасность, международный опыт регулирования (обзор). Безопасность и риск фармакотерапии. 2026;14(1):90-100. https://doi.org/10.30895/2312-7821-2026-14-1-90-100
For citation:
Kazakov R.E., Serebrova S.Yu., Esakova E.Yu., Zhuravleva M.V., Prokofiev A.B. Therapeutic and Prophylactic Bacteriophage Preparations: Efficacy, Safety, and International Regulatory Experience (Review). Safety and Risk of Pharmacotherapy. 2026;14(1):90-100. (In Russ.) https://doi.org/10.30895/2312-7821-2026-14-1-90-100
JATS XML