Перейти к:
Лекарственно-индуцированная аллергия у взрослых в многопрофильном стационаре: оценка распространенности методом глобальных триггеров
https://doi.org/10.30895/2312-7821-2025-481
Резюме
ВВЕДЕНИЕ. Лекарственно-индуцированные аллергические реакции (ЛИАР) у госпитализированных пациентов ограничивают возможности рациональной фармакотерапии и увеличивают риск полипрагмазии в связи с необходимостью коррекции состояния пациента и назначения противоаллергических препаратов. Объективная оценка частоты ЛИАР в стационаре и структуры препаратов для коррекции назначений является актуальной задачей, решение которой позволит как достичь значимого улучшения клинических исходов пациентов, так и снизить бремя затрат системы здравоохранения. Метод глобальных триггеров основан на анализе медицинской документации и фиксировании определенных триггеров, что делает его легко применимым в клинической практике.
ЦЕЛЬ. Изучение возможности использования метода глобальных триггеров для оценки распространенности ЛИАР у пациентов многопрофильного стационара.
МАТЕРИАЛЫ И МЕТОДЫ. Ретроспективное фармакоэпидемиологическое исследование медицинской документации пациентов, госпитализированных в ГБУЗ «Городская клиническая больница № 24 Департамента здравоохранения города Москвы» в период с 01.10.2022 по 01.04.2023, с использованием метода глобальных триггеров. Критерии включения: пациенты, проходившие стационарное лечение в отделениях терапевтического и хирургического профиля в указанный период. Критерии исключения: пациенты отделения аллергологии.
РЕЗУЛЬТАТЫ. Всего за анализируемый период в отделения терапевтического и хирургического профилей поступили 8934 пациента. Триггеры ЛИАР были идентифицированы у 229 (2,6%, то есть 2563 на 100 000 пациентов). Оценка листов назначений, дневников и клинико-лабораторных данных позволила выявить лишь 52 истинных триггера ЛИАР (22,7%). В оставшихся 177 случаях (77,3%) противоаллергический препарат был назначен до или одномоментно с подозреваемым лекарственным средством, предположительно с целью профилактики возможного развития аллергической реакции, что оценивали как ложный триггер. Основными группами подозреваемых препаратов явились антибактериальные средства для системного применения (22 препарата (40,7%), в частности бета-лактамные антибиотики — 14 препаратов (20,3%)), а также моноклональные антитела (21 препарат (38,9%)).
ВЫВОДЫ. Истинная частота развития ЛИАР составила 0,58% (582 на 100 000 пациентов). Продемонстрированные в исследовании результаты показали эффективность применения метода глобальных триггеров для выявления случаев лекарственной аллергии в реальной клинической практике. Исключение ложных триггеров (прежде всего профилактических назначений лекарственных препаратов) уменьшает искажение реальной частоты ЛИАР и гипердиагностики данного состояния.
Ключевые слова
Для цитирования:
Коваль В.Р., Бутранова О.И., Константинова Т.Г., Аль-Майяхи А. Лекарственно-индуцированная аллергия у взрослых в многопрофильном стационаре: оценка распространенности методом глобальных триггеров. Безопасность и риск фармакотерапии. 2025;13(3):313-323. https://doi.org/10.30895/2312-7821-2025-481
For citation:
Koval V.R., Butranova O.I., Konstantinova T.G., Al-Mayahi A. Drug Allergy in Adults at a Multidisciplinary Hospital: Prevalence Assessment Using the Global Trigger Tool. Safety and Risk of Pharmacotherapy. 2025;13(3):313-323. (In Russ.) https://doi.org/10.30895/2312-7821-2025-481
ВВЕДЕНИЕ
Нежелательная реакция (НР) — непреднамеренная неблагоприятная реакция организма, связанная с применением лекарственного препарата (ЛП) и предполагающая наличие взаимосвязи с применением подозреваемого лекарственного препарата1. НР наиболее распространены среди пациентов стационаров и возникают почти у 20% госпитализированных пациентов [1]. Согласно расчетам, основанным на данных глобального бремени болезней с 1990 по 2019 гг., стандартизированный по возрасту коэффициент смертности, связанной с НР, к 2040 г. составит 1,58 (95% интервал неопределенности: 1,33–1,80) [2]. По данным метаанализа 2024 г., затраты на ведение одного пациента с НР (одна госпитализация) в развитых странах варьируют от 6 до 10 тыс. евро [3], что отражает высокий уровень затрат системы здравоохранения в случае развития НР.
Своевременное выявление НР в условиях стационара является необходимым элементом повышения безопасности фармакотерапии. Существуют несколько валидированных методов, которые используются для выявления и оценки НР. Метод спонтанных сообщений основан на добровольных отчетах всех участников обращения ЛП о НР. Внедрение в практику метода спонтанных сообщений обеспечивает формирование базы данных о НР на уровне государства. Тем не менее данный метод имеет ограничения: показатели отчетности могут значительно варьировать в зависимости от мотивации репортера, наличия времени, квалификации, интерпретации значимости проблемы [4]. Также существует система активного мониторинга безопасности лекарственных средств, принципом которого является активное наблюдение после лечения, НР могут выявляться путем прямого опроса пациентов или скрининга медицинских карточек пациентов. Недостатком метода является относительно небольшое число пациентов [5]. Еще одним методом активного мониторинга является метод глобальных триггеров (Global Trigger Tool), разработанный в Институте совершенствования здравоохранения США (Institute for Healthcare Improvement, IHI), — это инструмент, включающий поиск специальных триггеров НР в истории болезни пациента, что позволяет в короткие сроки и с минимальными затратами оценить безопасность фармакотерапии, что особенно важно в случае лекарственно-индуцированных аллергических реакций (ЛИАР) [6].
Триггерами возможного развития ЛИАР у госпитализированных пациентов могут быть резкая отмена или смена ЛП, назначение таких препаратов, как блокаторы Н1-гистаминовых рецепторов, адреналин, топические стероиды, внутривенное введение глюкокортикостероидов, а также записи о характерных симптомах аллергической реакции в дневниках наблюдения.
ЛИАР могут составлять до трети всех случаев НР в отделениях, оказывающих неотложную помощь [7]. Наиболее распространенной группой ЛП, вызывающей ЛИАР, являются антибактериальные препараты [1]. По данным метаанализа 32 исследований (n=1 089 675) распространенность зарегистрированных случаев ЛИАР, индуцированных антибактериальными препаратами, составляет от 5 до 35% [8]. Факторы риска включают наличие любых ЛИАР в анамнезе, повторное назначение подозреваемого ЛП, а также параллельное назначение препаратов некоторых других групп (например, ингибиторов ангиотензинпревращающего фермента) [9], принадлежность к женскому полу [10]. Важная роль в развитии ЛИАР принадлежит также полипрагмазии [11].
В то же время избыточная диагностика ЛИАР, в частности вызванной антибиотиками, значимо ограничивает возможности лечащего врача и способствует распространению антибиотикорезистентности за счет включения в схемы терапии альтернативных препаратов, что указывает на необходимость активного изучения истинной распространенности ЛИАР [12].
Цель работы — изучить возможности использования метода глобальных триггеров для оценки распространенности ЛИАР у пациентов многопрофильного стационара.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено ретроспективное фармакоэпидемиологическое исследование медицинской документации пациентов, госпитализированных в Государственное бюджетное учреждение здравоохранения города Москвы «Городская клиническая больница № 24 Департамента здравоохранения города Москвы» в период с 01.10.2022 по 01.04.2023, с использованием метода глобальных триггеров.
Анализировали медицинские карты стационарных больных, отвечающие следующим критериям включения: закрытые и полностью заполненные истории болезни (включающие выписной эпикриз) пациентов отделений терапевтического (кардиология, терапия, неврология) и хирургического (гинекология, общая хирургия, колопроктология и урология) профилей; длительность пребывания пациента в стационаре не менее 72 ч; возраст пациента 18 лет и старше; назначение ЛП, относящихся к группе антигистаминных средств (код АТХ: R062) и кортикостероидов системного действия (код АТХ: H023). Критерий исключения: медицинские карты пациентов аллергологического отделения вследствие невозможности дифференцировки НР от базового лечения основного заболевания.
Триггеры ЛИАР оценивали с помощью двух из шести модулей метода глобальных триггеров: «Модуль I. Уход и наблюдение за пациентом», «Модуль II. Медикаментозное лечение» [13]. Триггерами считали 1) «назначение дифенгидрамина», обобщив в данном пункте назначения других противоаллергических ЛП: антигистаминных препаратов, кальция глюконата; 2) назначение глюкокортикостероидов, так как их чаще всего используют в реальной клинической практике для купирования симптомов аллергической реакции.
За анализируемый период в отделения, где проводили исследование, поступило 8934 пациента. Медицинские карты анализировали независимо друг от друга три исследователя, обладающие клиническими знаниями и опытом. Триггеры ЛИАР выявили в 229 историях болезни.
Средний возраст пациентов, в историях болезни которых были выявлены триггеры ЛИАР (n=229), составил 53,2±19,5 года, 48% (n=111) пациентов были старше 60 лет (табл. 1).
Таблица 1. Характеристика пациентов, в историях болезни которых были выявлены триггеры лекарственно-индуцированных аллергических реакций (n=229)
Table 1. Profile of patients with allergic drug reaction triggers identified in medical records (n=229)
Параметр Parameter | Значение Value |
Возраст (М±SD (min; max)), годы Age (М±SD (min; max)), years | 53,2±19,5 (18,0; 91,0) |
Женский пол, n (%) Female, n (%) | 139 (60,7) |
Индекс массы тела (М±SD (min; max)), кг/м² Body mass index (М±SD (min; max)), kg/m² | 27,1±6,5 (16,4; 52,0) |
Длительность госпитализации (М±SD (min; max)), сут Inpatient treatment duration (М±SD (min; max)), days | 7,5±3,7 (3,0; 35,0) |
Сопутствующие заболевания Comorbidity | |
Сердечно-сосудистые заболевания, n (%) Cardiovascular diseases, n (%) | 77 (33,6) |
Заболевания почек, n (%) Kidney diseases, n (%) | 15 (6,5) |
Сахарный диабет, n (%) Diabetes mellitus, n (%) | 22 (9,6) |
Нарушение функции печени, n (%) Liver dysfunction, n (%) | 14 (6,1) |
Онкология, n (%) Cancer, n (%) | 28 (12,2) |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
Примечание. M — среднее; SD — стандартное отклонение.
Note. M, mean; SD, standard deviation.
При обнаружении триггера в перечне медикаментозных назначений данные медицинской документации (дневники, совместные осмотры, анамнез жизни и основного заболевания, данные лабораторных и инструментальных методов диагностики) подвергали тщательному анализу для подтверждения наступления НР, оценки причиненного здоровью пациента вреда и идентификации собственно ЛИАР. ЛИАР классифицировали в соответствии с правилами кодирования Медицинского словаря терминов для регуляторной деятельности (Medical Dictionary for Regulatory Activities, MedDRA), версия 27.0 (март 2024 г.)4.
Анализ медицинской документации позволил разделить все выявленные триггеры на две группы: истинные и ложные. К ложным триггерам относили: 1) назначение противоаллергических препаратов пациентам при отсутствии описания симптомов аллергических реакций в истории болезни (данные ежедневных записей: дневник, описания обходов и совместных осмотров различными специалистами) или их признаков по данным лабораторной диагностики (нормальное содержание эозинофилов крови); 2) назначение триггерного препарата до или одновременно с назначением антибактериальных препаратов, нестероидных противовоспалительных средств, препаратов для наркоза и местных анестетиков. Истинными триггерами считали назначение противоаллергических препаратов через несколько часов или суток после начала введения подозреваемого препарата, а также назначение препаратов, на фоне применения которых у пациента проявились признаки аллергической реакции, отмеченные в медицинской документации.
Статистический анализ результатов исследования проводили с использованием программного обеспечения Microsoft Excel 2019. Анализ количественных показателей осуществляли методами описательной статистики: качественные переменные описывали при помощи абсолютных (n) и относительных (%) величин, данные проверяли на соответствие закону нормального распределения с помощью критерия Шапиро–Уилка. В исследовании все величины имели нормальное распределение, поэтому для них были рассчитаны: среднее (М) и стандартное отклонение (SD). Также был использован параметр положительного предиктивного значения (positive predictive value, PPV)5.
РЕЗУЛЬТАТЫ
Анализ 8934 историй болезни позволил выявить наличие триггеров в 229 (2,6%, то есть 2563 на 100 000 пациентов) случаях. Общее число идентифицированных триггерных назначений составило 254. Среди триггерных препаратов (табл. 2) преобладали блокаторы H1-гистаминовых рецепторов: 96,9% (n=246). Глюкокортикостероиды были назначены в 2,8% (n=7), кальция глюконат — в 0,4% (n=1).
Таблица 2. Перечень выявленных триггерных препаратов
Table 2. List of the identified trigger medicinal products
Международное непатентованное наименование (МНН) International Non-proprietary Name (INN) | Количество Quantity | |
n | % | |
Блокаторы H1-гистаминовых рецепторов (всего) / H1-histamine receptor blockers (total) | 246 | 96,9 |
Хлоропирамин/Chloropyramine | 68 | 26,8 |
Клемастин/Clemastine | 139 | 54,7 |
Гидроксизин/Hydroxyzine | 9 | 3,5 |
Цетиризин/Cetirizine | 25 | 9,8 |
Мебгидролин/Mebhydroline | 5 | 2,0 |
Глюкокортикостероиды (всего) / Glucocorticoids (total) | 7 | 2,8 |
Дексаметазон/Dexamethasone | 2 | 0,8 |
Преднизолон/Prednisolone | 5 | 2,0 |
Прочие (кальция глюконат) / Other (сalcium gluconate) | 1 | 0,4 |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
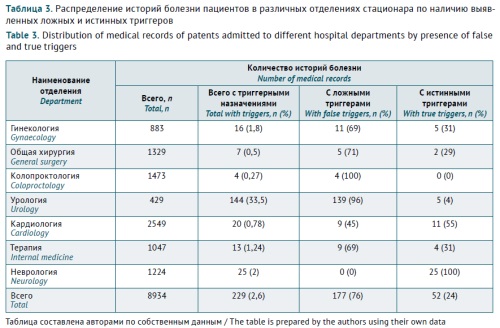
Общее число историй болезни с истинными триггерами, которые могли привести к развитию НР, составило 52 (22,7%; PPV=20,47%). В 77,3% (n=177) историй болезни триггерные препараты были назначены для профилактики возможного развития аллергических реакций; такие триггеры определены как ложные (табл. 3).
Таблица 3. Распределение историй болезни пациентов в различных отделениях стационара по наличию выявленных ложных и истинных триггеров
Table 3. Distribution of medical records of patents admitted to different hospital departments by presence of false and true triggers
Наименование отделения Department | Количество историй болезни Number of medical records | |||
Всего, n Total, n | Всего с триггерными назначениями Total with triggers, n (%) | С ложными триггерами With false triggers, n (%) | С истинными триггерами With true triggers, n (%) | |
Гинекология Gynaecology | 883 | 16 (1,8) | 11 (69) | 5 (31) |
Общая хирургия General surgery | 1329 | 7 (0,5) | 5 (71) | 2 (29) |
Колопроктология Coloproctology | 1473 | 4 (0,27) | 4 (100) | 0 (0) |
Урология Urology | 429 | 144 (33,5) | 139 (96) | 5 (4) |
Кардиология Cardiology | 2549 | 20 (0,78) | 9 (45) | 11 (55) |
Терапия Internal medicine | 1047 | 13 (1,24) | 9 (69) | 4 (31) |
Неврология Neurology | 1224 | 25 (2) | 0 (0) | 25 (100) |
Всего Total | 8934 | 229 (2,6) | 177 (76) | 52 (24) |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
Следующий этап работы был направлен на оценку аллергологического анамнеза в группах с истинными и ложными триггерами. Анализ медицинской документации всех пациентов выявил лекарственную аллергию в анамнезе у 14% (33/229).
Среднее количество принимаемых препаратов на одного пациента в группе истинных триггеров составило 6,9±3,2 (min — 2; max — 15).
При анализе клинической картины, сопровождавшей развитие ЛИАР в группе с истинными триггерами, выявлено 58 НР (классификация по первичным системно-органным классам MedDRA): нарушения со стороны кожи и подкожной клетчатки — сыпь, крапивница (70,7%, n=41), эритема (5,2%, n=3); общие нарушения и реакции в месте введения — зуд и покраснение кожи в месте введения препарата (18,9%, n=11); нарушения со стороны иммунной системы — анафилактоидная реакция (3,4%, n=2); нарушения со стороны дыхательной системы, органов грудной клетки и средостения — бронхоспазм (1,7%, n=1). Бóльшая часть выявленных НР (94,8%, 55/58) носила несерьезный характер (временный вред здоровью).
После анализа листов назначений пациентов группы с истинными триггерами был составлен перечень подозреваемых в развитии ЛИАР препаратов из 130 наименований (среднее значение на одного пациента 2,5±1,2 (1; 6)). Опираясь на заключения лечащих врачей, клинических фармакологов и данные консультаций аллергологов-иммунологов, перечень подозреваемых в развитии ЛИАР препаратов был сокращен до 54 (табл. 4).
Таблица 4. Перечень препаратов, подозреваемых в развитии лекарственно-индуцированных аллергических реакций при выявлении истинных триггеров по данным историй болезни
Table 4. List of medicinal products suspected to cause allergic drug reactions in patients with true triggers identified in medical records
Препараты Medicinal products (n=54) | Количество Quantity | |
n | % | |
Антибактериальные препараты / Antimicrobial agents | 22 | 40,7 |
Цефалоспорины/Cephalosporins | 11 | 20,3 |
Фторхинолоны/Fluoroquinolones | 5 | 9,2 |
Аминогликозиды/Aminoglycosides | 1 | 1,9 |
Гликопептиды/Glycopeptides | 1 | 1,9 |
Карбапенемы/Carbapenems | 1 | 1,9 |
Монобактам/Monobactams | 1 | 1,9 |
Оксазолидиноны/Oxazolidinones | 1 | 1,9 |
Пенициллины/Penicillins | 1 | 1,9 |
Моноклональные антитела / Monoclonal antibodies | 21 | 38,8 |
Нестероидные противовоспалительные препараты / Nonsteroidal anti-inflammatory drugs | 2 | 3,7 |
Амиодарон/Amiodarone | 1 | 1,9 |
Аторвастатин/Atorvastatin | 1 | 1,9 |
Ацетилцистеин/Acetylcysteine | 1 | 1,9 |
Железо-сахарозный комплекс / Iron–sugar complex | 1 | 1,9 |
Оксалиплатин/Oxaliplatin | 1 | 1,9 |
Спиронолактон/Spironolactone | 1 | 1,9 |
Флуконазол/Fluconazole | 1 | 1,9 |
Флуоксетин/Fluoxetine | 1 | 1,9 |
Эмпаглифлозин/Empagliflozin | 1 | 1,9 |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
Основными подозреваемыми в развитии ЛИАР были две группы препаратов: системные антибактериальные средства — 40,7% (22/54), преимущественно бета-лактамы 63,6% (14/22), и моноклональные антитела — 38,9% (21/54). Ввиду необходимости применения того или иного ЛП в большинстве случаев врачам приходилось продолжать терапию, используя противоаллергические ЛП. Отмена/смена ЛП выявлена лишь в 7,4% случаев (4/54).
При выявлении ложных триггеров в 92,1% (163/177) случаев назначение противоаллергических ЛС, вероятно, было связано с профилактикой развития аллергической реакции на фоне приема антибактериальных препаратов, в частности из групп цефалоспоринов — 90 (50,9%) и фторхинолонов — 84 (47,5%).
Средняя длительность госпитализации пациентов в группе с истинными триггерами составила 8,5 сут. Более подробная характеристика приведена в таблице 5.
Таблица 5. Характеристика пациентов, в историях болезни которых были выявлены истинные триггеры лекарственно-индуцированных аллергических реакций (n=52)
Table 5. Profile of patients with true allergic drug reaction triggers identified in medical records (n=52)
Параметр Parameter | Значение Value |
Возраст (М±SD (min; max)), годы Age (М±SD (min; max)), years | 48,8±20,2 (18,0; 91,0) |
Количество пациентов >60 лет, n (%) Number of patients >60 years, n (%) | 20 (38,5) |
Женский пол, n (%) Female sex, n (%) | 32 (61,5) |
Индекс массы тела (М±SD (min; max)), кг/м² Body mass index (М±SD (min; max)), kg/m² | 26,8±6,05 (18,2; 44,0) |
Индекс массы тела >30 кг/м², % Body mass index >30 kg/m², % | 27% |
Длительность госпитализации (М±SD (min; max)), сут Inpatient treatment duration (М±SD (min; max)), days | 8,5±4,7 (3,0; 35,0) |
Сердечно-сосудистые заболевания, n (%) Cardiovascular diseases, n (%) | 19 (36,5) |
Заболевания почек, n (%) Kidney diseases, n (%) | 5 (9,6) |
Сахарный диабет, n (%) Diabetes mellitus, n (%) | 2 (3,8) |
Нарушение функции печени, n (%) Liver dysfunction, n (%) | 3 (5,8) |
Онкология, n (%) Cancer, n (%) | 8 (15,4) |
Таблица составлена авторами по собственным данным / The table is prepared by the authors using their own data
ОБСУЖДЕНИЕ
С помощью метода глобальных триггеров нами было обнаружено 2,6% (229/8934) медицинских карт стационарных больных, у которых в период госпитализации могли развиться ЛИАР. Это значительно ниже уровня ЛИАР, приведенного в опубликованных данных (15–20% для госпитализированных пациентов) [1], но в целом соответствует результатам, представленным в работе по использованию метода глобальных триггеров для идентификации НР: общая распространенность НР — 13,39%, при этом доля аллергических реакций (были представлены кожные НР), — около 2,4% среди всех пациентов [14].
Факторами риска развития ЛИАР, по данным литературы, являются эпизоды ЛИАР в анамнезе, полипрагмазия и принадлежность к женскому полу [9–11][15]. Установленные нами характеристики пациентов с ЛИАР, развившимися в результате воздействия истинных триггеров, соответствуют данной картине [16–19]: лекарственная аллергия в анамнезе имелась в 57,7% (30/52) случаев. Преобладали пациенты женского пола (61,5%). Известно, что женский пол установлен как один из факторов риска различных форм ЛИАР. Например, среди взрослых пациенток риск аллергии на пенициллин в 10 раз выше, чем у мужчин [20]. Кожные ЛИАР, включая тяжелые, также чаще развиваются у пациентов женского пола [21][22].
У пациентов с ЛИАР среднее число препаратов составило 6,9±3,2. При назначении более 5 ЛП риск развития НР резко возрастает [23]. Проспективное исследование, проведенное в Великобритании (n=218, период наблюдения — 1 мес.) показало, что в группе госпитализированных пациентов с развившимися НР среднее количество препаратов, принимаемых одним пациентом, составило 10,5±4,6 по сравнению с 7,8±5,1 для пациентов без НР; полипрагмазия была выявлена у 91% в группе с НР и у 73% в группе без НР [24]. Следует также учитывать, что от 1 до 10% людей с лекарственной аллергией имеют синдром множественной лекарственной непереносимости (непереносимость 3 и более структурно и фармакологически не связанных ЛП), что в условиях полипрагмазии способствует дополнительному повышению риска ЛИАР [25]. Значимым фактором профилактики ЛИАР является плановое и контролируемое снижение числа назначаемых пациенту препаратов — депрескрайбинг, один из важных инструментов повышения безопасности фармакотерапии [26].
В проведенном исследовании средняя продолжительность госпитализации пациентов, для которых были выявлены истинные триггеры ЛИАР, составила 8,5±4,7 сут. В работе [27] была продемонстрирована значительно бóльшая длительность госпитализации (средняя разница 3,98 сут; 95% ДИ: от 2,91 до 5,05 сут). Максимальное увеличение длительности госпитализации вследствие НР характерно для пациентов пожилого и старческого возраста (12,4±11,0 сут против 7,3±6,4 сут у пациентов без НР; p<0,0001) [28]. Кроме того, продление госпитализации является фактором, способствующим увеличению затрат системы здравоохранения. Российские исследователи оценили экономические затраты на нежелательные лекарственные реакции при проведении терапии и выявили, что в структуре прямых медицинских затрат коррекция НР занимает от 1 до 10% от общих затрат на лечение [29].
Большинство препаратов, подозреваемых в развитии ЛИАР в проведенном исследовании, относились к антибактериальным средствам для системного применения (40,7%, n=22), в частности бета-лактамным антибиотикам (20,3%, n=14), а также к моноклональным антителам (38,9%, n=21). ЛП этих групп являются типичными причинами развития ЛИАР [8][30]. Распространенность ЛИАР, вызванных бета-лактамами, в частности пенициллинами, достигает 10% [9][30]. По данным российской национальной базы фармаконадзора (период 02.04.2019–21.06.2023) развитие лекарственно-индуцированной анафилаксии было связано с применением бета-лактамов почти в 88% случаев [31]. В качестве причины тяжелых кожных ЛИАР (синдром Стивенса–Джонсона, токсический эпидермальный некролиз) по результатам анализа российской национальной базы данных фармаконадзора (период 01.04.2019–31.12.2023) бета-лактамы были идентифицированы в 61% случаев [32]. Современные данные свидетельствуют о возрастающей роли моноклональных антител в развитии ЛИАР. В частности, они были выявлены в качестве второй по значимости причины анафилаксии в США (база данных FAERS, период 1999–2019 гг.) после антибактериальных препаратов; при этом темпы роста числа сообщений об анафилаксии вследствие приема моноклональных антител были максимальными среди всех фармакологических классов [33]. Аналогично максимальная скорость роста удельной доли сообщений среди всех фармакологических классов была выявлена для моноклональных антител и в случае лекарственно-индуцированных тяжелых кожных аллергических реакций (синдром Стивенса—Джонсона и токсический эпидермальный некролиз): в 2004 г. в базе данных FAERS не было ни одного сообщения, 2021 г. — 4,79% [34].
Для профилактики реакций гиперчувствительности в стационаре непосредственно перед применением препарата, обладающего высоким риском развития ЛИАР, могут назначаться блокаторы Н1-, Н2-рецепторов гистамина и глюкокортикоиды. Данный метод используется в случае установленной аллергии на препарат при невозможности заменить его на альтернативный [35]. Однако для предотвращения необоснованного назначения ЛП и связанной с этим полипрагмазии необходимо дополнительно привлекать врачей клинических фармакологов и аллергологов.
К ограничениям проведенного исследования относятся: исследование выборки пациентов на базе только одного медицинского учреждения, узкий временной промежуток, а также отсутствие сравнения данных с группой пациентов без НР. Следующие этапы исследования планируется осуществлять, расширяя временной промежуток для получения большего объема данных и увеличения выборки пациентов. Также запланировано изучение возможности применения метода глобальных триггеров для оценки общей структуры НР среди госпитализированных пациентов.
ЗАКЛЮЧЕНИЕ
В ретроспективном исследовании с использованием метода глобальных триггеров 8934 медицинских карт на базе многопрофильного стационара триггеры ЛИАР были идентифицированы в 2,6% случаев (2563 на 100 000 пациентов). Анализ листов назначений, дневников и клинико-лабораторных данных позволил исключить ложные триггеры (профилактическое назначение противоаллергических препаратов) и выявить истинную частоту развития ЛИАР — 0,58% (582 на 100 000 пациентов).
Основными группами подозреваемых в развитии ЛИАР препаратов являлись системные антибактериальные средства (40,7%, в частности бета-лактамные антибиотики — 20,3%), а также моноклональные антитела (38,9%).
Продемонстрированные в исследовании результаты показали эффективность применения метода глобальных триггеров для выявления случаев лекарственной аллергии в реальной клинической практике. Исключение ложных триггеров (прежде всего профилактических назначений ЛП) уменьшает искажение реальной частоты ЛИАР и гипердиагностики данного состояния.
Вклад авторов. Все авторы подтверждают соответствие своего авторства критериям ICMJE. Наибольший вклад распределен следующим образом: В.Р. Коваль — сбор и анализ информации, написание текста рукописи, формулировка выводов, работа с источниками литературы; О.И. Бутранова — участие в формулировке выводов, утверждение окончательной версии рукописи для публикации; Т.Г. Константинова — сбор и анализ информации; А.К.Ш. Аль-Маяхи — сбор и анализ информации.
Соответствие принципам этики. Авторы заявляют, что одобрение комитетом по этике не требовалось, поскольку были проанализированы обезличенные данные медицинских карт (архивные материалы), и в исследовании непосредственно не участвовали люди.
Authors’ contributions. All authors confirm that they meet the ICMJE criteria of authorship. The most significant contributions were as follows. Victoria R. Koval collected and analysed information, drafted the manuscript, formulated the conclusions, and worked with literature sources. Olga I. Butranova formulated the conclusions and approved the final version of the manuscript for publication. Tatiana G. Konstantinova collected and analysed information. Ahmed Q.S. Al-Mayahi collected and analysed information.
Ethics approval. According to the authors, the analysis was based on previously published anonymised data (archived medical records), and the study did not involve direct participation of human subjects. Hence, this study is exempt from ethics approval.
1. Решение Совета Евразийской экономической комиссии от 03.11.2016 № 87 «Об утверждении Правил надлежащей практики фармаконадзора Евразийского экономического союза».
2. Код АТХ R06A | Антигистаминные средства системного действия | АТХ классификация лекарственных средств 2025.
3. Код АТХ H02 | Кортикостероиды системного действия | АТХ классификация лекарственных средств 2025.
4. Medical Dictionary for Regulatory Activities – MedDRA.
5. PPV — статистический показатель, отражающий вероятность наличия исследуемого состояния у пациента с положительным результатом теста (доля истинно положительных результатов среди всех положительных результатов теста). Значения PPV ниже 50% обычно считаются низкими, так как в таких случаях более половины положительных результатов теста являются ложными. PPV будет низким при низкой распространенности (даже если тест имеет хорошую точность) и высоким при высокой распространенности.
Список литературы
1. Doña I, Torres MJ, Celik G, Phillips E, Tanno LK, Castells M. Changing patterns in the epidemiology of drug allergy. Allergy. 2024;79(3):613–28. https://doi.org/10.1111/all.15970
2. Kong X, Tao X, Li L, Zhao X, Ren J, Yang S, et al. Global trends and partial forecast of adverse effects of medical treatment from 1990 to 2019: An epidemiological analysis based on the Global Burden of Disease Study 2019. BMC Public Health. 2024;24(1):295. https://doi.org/10.1186/s12889-023-17560-0
3. Durand M, Castelli C, Roux-Marson C, Kinowski JM, Leguelinel-Blache G. Evaluating the costs of adverse drug events in hospitalized patients: A systematic review. Health Econ Rev. 2024;14(1):11. https://doi.org/10.1186/s13561-024-00481-y
4. Johansson ML, Hägg S, Wallerstedt SM. Impact of information letters on the reporting rate of adverse drug reactions and the quality of the reports: A randomized controlled study. BMC Clin Pharmacol. 2011;11:14. https://doi.org/10.1186/1472-6904-11-14
5. Журавлева МВ, Сереброва СЮ, Кузнецова ЕВ, Каменева ТР, Власова АВ, Прокофьев АБ, Демченкова ЕЮ. Совершенствование системы фармаконадзора в медицинских организациях как возможность повышения качества фармакотерапии. Безопасность и риск фармакотерапии. 2025;13(1): 94–107. https://doi.org/10.30895/2312-7821-2025-13-1-94-107
6. Moraes SM, Ferrari TCA, Beleigoli A. The accuracy of the Glo bal Trigger Tool is higher for the identification of adverse events of greater harm: A diagnostic test study. Int J Qual Health Care. 2023;34(1):mzad005. https://doi.org/10.1093/intqhc/mzad005
7. Kiechle ES, McKenna CM, Carter H, Zeymo A, Gelfand BW, DeGeorge LM, et al. Medication allergy and adverse drug reaction documentation discrepancies in an urban, academic emergency department. J Med Toxicol. 2018;14(4):272–7. https://doi.org/10.1007/s13181-018-0671-7
8. Arnold A, Coventry LL, Foster MJ, Koplin JJ, Lucas M. The burden of self-reported antibiotic allergies in health care and how to address it: A systematic review of the evidence. J Allergy Clin Immunol Pract. 2023;11(10):3133-3145.e3. https://doi.org/10.1016/j.jaip.2023.06.025
9. Park CS, Yang MS, Kang DY, Park HJ, Park SY, Nam YH, et al. Drug Allergy Work Group of KAAACI. Risk factors of beta-lactam anaphylaxis in Korea: A 6-year multicenter retrospective adult case-control study. World Allergy Organ J. 2021;14(9):100580. https://doi.org/10.1016/j.waojou.2021.100580
10. Miller MA. Gender-based differences in the toxicity of pharmaceuticals — the Food and Drug Administration’s perspective. Int J Toxicol. 2001;20(3):149–52. https://doi.org/10.1080/109158101317097728
11. Thong BY, Tan TC. Epidemiology and risk factors for drug allergy. Br J Clin Pharmacol. 2011;71(5):684–700. https://doi.org/10.1111/j.1365-2125
12. Macy E. Addressing the epidemic of antibiotic “allergy” over-diagnosis. Ann Allergy Asthma Immunol. 2020;124(6):550–7. https://doi.org/10.1016/j.anai.2019.12.016
13. Скрябина АА, Терешкин НА, Никифоров ВВ, Каширин ВИ, Антипят НА, Застрожин МС, Сычев ДА. Применение метода глобальных триггеров для выявления нежелательных лекарственных реакций у пациентов стационара инфекционного профиля. Медицина. 2023;11(2):42–55. https://doi.org/10.29234/2308-9113-2023-11-2-42-55
14. Pandya AD, Patel K, Rana D, Gupta SD, Malhotra SD, Patel P. Global Trigger Tool: Proficient adverse drug reaction autodetection method in critical care patient units. Indian J Crit Care Med. 2020;24(3):172–8. https://doi.org/10.5005/jp-journals-10071-23367
15. Pallardy M, Bechara R, Whritenour J, Mitchell-Ryan S, Herzyk D, Lebrec H, et al. Drug hypersensitivity reactions: Review of the state of the science for prediction and diagnosis. Toxicol Sci. 2024;200(1):11–30. https://doi.org/10.1093/toxsci/kfae046
16. Rodríguez-Pérez R, de las Vecillas L, Cabañas R, Bellón T. Tools for etiologic diagnosis of drug-induced allergic conditions. Int J Mole cular Sciences. 2023;24(16):12577. https://doi.org/10.3390/ijms241612577
17. Lee EY, Copaescu AM, Trubiano JA, Phillips EJ, Wolfson AR, Ramsey A. Drug allergy in women. J Allergy Clin Immunol Pract. 2023;11(12):3615–23. https://doi.org/10.1016/j.jaip.2023.09.031
18. Сабанцева ЕГ, Иванова ЕВ, Рабинович ИМ. Проявления аллергических реакций, возникающих на стоматологическом приеме. Стоматология. 2021;100(6–2):29–32. https://doi.org/10.17116/stomat202110006229
19. de Vries ST, Denig P, Ekhart C, Burgers JS, Kleefstra N, Mol PGM, et al. Sex differences in adverse drug reactions reported to the National Pharmacovigilance Centre in the Netherlands: An explorative observational study. Br J Clin Pharmacol. 2019;85(7):1507–15. https://doi.org/10.1111/bcp.13923
20. Voelker DH, Gonzalez-Estrada A, Park MA. Female sex as a risk factor for penicillin drug allergy in the inpatient setting. Allergy Asthma Proc. 2022;43(2):163–7. https://doi.org/10.2500/aap.2022.43.210002
21. Mizukawa Y, Hama N, Miyagawa F, Takahashi H, Ogawa Y, Kurata M, et al. Drug-induced hypersensitivity syndrome/drug reaction with eosinophilia and systemic symptoms: Predictive score and outcomes. J Allergy Clin Immunol Pract. 2023;11(10):3169-3178.e7. https://doi.org/10.1016/j.jaip.2023.06.065
22. Li D, Gou J, Zhu J, Zhang T, Liu F, Zhang D, et al. Severe cutaneous adverse reactions to drugs: A real-world pharmacovigilance study using the FDA Adverse Event Reporting System database. Front Pharmacol. 2023;14:1117391. https://doi.org/10.3389/fphar.2023.1117391
23. Сычев ДА, Отделенов ВА, Краснова НМ, Ильина ЕС. Полипрагмазия: взгляд клинического фармаколога. Терапевтический архив. 2016;88(12):94–102. Sychev DA, Otdelеnov VA, Krasnova NM, Ilyina ES. Polypragmasy: A clinical pharmacologist’s view. Therapeutic Archive. 2016;88(12):94–102 (In Russ.). https://doi.org/10.17116/terarkh2016881294-102
24. Osanlou R, Walker L, Hughes DA, Burnside G, Pirmohamed M. Adverse drug reactions, multimorbidity and polypharmacy: A prospective analysis of 1 month of medical admissions. BMJ Open. 2022;12(7):e055551. https://doi.org/10.1136/bmjopen-2021-055551
25. Ferranti J, Horvath M, Cozart H, Whitehurst J, Eckstrand J, Pietrobon R, et al. A multifaceted approach to safety: The synergistic detection of adverse drug events in adult inpatients. J Patient Saf. 2008;4(3):184–190. https://doi.org/10.1097/PTS.0b013e318184a9d5
26. Reeve J, Maden M, Hill R, Turk A, Mahtani K, Wong G, et al. Deprescribing medicines in older people living with multimorbidity and polypharmacy: The TAILOR evidence synthesis. Health Technol Assess. 2022;26(32):1–148. https://doi.org/10.3310/AAFO2475
27. Patel TK, Patel PB, Bhalla HL, Dwivedi P, Bajpai V, Kishore S. Impact of suspected adverse drug reactions on mortality and length of hospital stay in the hospitalised patients: A meta-analysis. Eur J Clin Pharmacol. 2023;79(1):99–116. https://doi.org/10.1007/s00228-022-03419-7
28. Sandoval T, Martínez M, Miranda F, Jirón M. Incident adverse drug reactions and their effect on the length of hospital stay in older inpatients. Int J Clin Pharm. 2021;43(4):839–46. https://doi.org/10.1007/s11096-020-01181-3
29. Крысанова ВС, Крысанов ИС, Журавлева МВ, Гуревич КГ, Ермакова ВЮ. Оценка экономических затрат на нежелательные лекарственные реакции при проведении терапии. Фармация. 2018;67(8):44–50. https://doi.org/10.29296/25419218-2018-08-07
30. Buffone B, Lin YC, Grant J. β-lactam exposure outcome among patients with a documented allergy to penicillins post-implementation of a new electronic medical record system and alerting rules. J Assoc Med Microbiol Infect Dis Can. 2021;6(2):104–13. https://doi.org/10.3138/jammi-2020-0050
31. Butranova O, Zyryanov S, Gorbacheva A, Asetskaya I, Polivanov V. Drug-induced anaphylaxis: National database analysis. Pharmaceuticals. 2024;17(1):90. https://doi.org/10.3390/ph17010090
32. Zyryanov S, Asetskaya I, Butranova O, Terekhina E, Polivanov V, Yudin A, et al. Stevens–Johnson syndrome and toxic epidermal necro lysis: Analysis of the Russian database of spontaneous reports. Pharmaceuticals. 2024;17(6):675. https://doi.org/10.3390/ph17060675
33. Yu RJ, Krantz MS, Phillips EJ, Stone CA Jr. Emerging causes of drug-induced anaphylaxis: A review of anaphylaxis-associated reports in the FDA Adverse Event Reporting System (FAERS). J Allergy Clin Immunol Pract. 2021;9(2):819–29.e2. https://doi.org/10.1016/j.jaip.2020.09.021
34. Fei W, Shen J, Cai H. Causes of drug-induced severe cutaneous adverse reaction epidermal necrolysis (EN): An analysis using FDA Adverse Event Reporting System (FAERS) database. Clin Cosmet Investig Dermatol. 2023;16:2249–57. https://doi.org/10.2147/CCID.S422928
35. Kang SY, Seo J, Kang HR. Desensitization for the prevention of drug hypersensitivity reactions. Korean J Intern Med. 2022;37(2):261–70. https://doi.org/10.3904/kjim.2021.438
Об авторах
В. Р. КовальРоссия
Коваль Виктория Рустамовна
ул. Миклухо-Маклая, д. 6, Москва, 117198
О. И. Бутранова
Россия
Бутранова Ольга Игоревна, канд. мед. наук, доцент
ул. Миклухо-Маклая, д. 6, Москва, 117198
Т. Г. Константинова
Россия
Константинова Татьяна Геннадьевна
ул. Миклухо-Маклая, д. 6, Москва, 117198
А.К.Ш. Аль-Майяхи
Россия
Аль-Майяхи Ахмед Касим Шархан
ул. Миклухо-Маклая, д. 6, Москва, 117198
Дополнительные файлы
Рецензия
Для цитирования:
Коваль В.Р., Бутранова О.И., Константинова Т.Г., Аль-Майяхи А. Лекарственно-индуцированная аллергия у взрослых в многопрофильном стационаре: оценка распространенности методом глобальных триггеров. Безопасность и риск фармакотерапии. 2025;13(3):313-323. https://doi.org/10.30895/2312-7821-2025-481
For citation:
Koval V.R., Butranova O.I., Konstantinova T.G., Al-Mayahi A. Drug Allergy in Adults at a Multidisciplinary Hospital: Prevalence Assessment Using the Global Trigger Tool. Safety and Risk of Pharmacotherapy. 2025;13(3):313-323. (In Russ.) https://doi.org/10.30895/2312-7821-2025-481