ОСНОВНАЯ ИНФОРМАЦИЯ О ЖУРНАЛЕ
«Безопасность и риск фармакотерапии» – научно-практический рецензируемый журнал открытого доступа, выпускаемый в печатной и онлайн-версиях, единственный в России, полностью посвященный данной тематике. Основан в 1994 году.
Цель журнала: освещение научных достижений и практического опыта в области обеспечения безопасности лекарственных средств и снижения рисков фармакотерапии.
Целевая аудитория. Предназначен для специалистов практического здравоохранения, клинических фармакологов и врачей других специальностей, провизоров, специалистов экспертных учреждений, уполномоченных по фармаконадзору и специалистов по фармаконадзору фармацевтических компаний и организаций, сотрудников центров доклинических и клинических исследований, регуляторных и контрольно-надзорных органов в сфере обращения лекарственных средств, научно-исследовательских институтов, преподавателей, студентов и соискателей медицинских и фармацевтических вузов. Более подробная информация – в разделе «Цели и тематика».
Учредитель: ФГБУ «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации.
Периодичность: 4 раза в год.
Импакт-фактор: двухлетний импакт-фактор РИНЦ (2024) - 0,826.
Редколлегия. Географическое представительство:
- 3 континента
- 10 стран
- 17 городов
Рецензирование:
- Двойное слепое
- Минимум 2 рецензента на рукопись
Основные метрики журнала:
- 14 дней в среднем от подачи до первого решения
- 151 день в среднем от подачи до публикации в Интернете
- 23% приглашенных авторов
- 63% доля принятия рукописей
- 37 тыс. загрузок PDF в 2023 г.
Плата за публикацию: бесплатно.
Индексация. Входит в Scopus (Accepted Titles May 2025), Перечень ВАК (категория К1), Russian Science Citation Index, РИНЦ, DOAJ seal. Информация об индексации в других российских и международных базах доступна в разделе Индексирование.
Регистрация. Свидетельство о регистрации средства массовой информации ПИ № ФС77-82932 от 14 марта 2022 г.
Подписка. Подписной индекс в каталоге Пресса России – 57940, Урал-Пресс – 57940.
Текущий выпуск
ГЛАВНАЯ ТЕМА: ЭВОЛЮЦИЯ ФАРМАКОНАДЗОРА: ИНТЕГРАЦИЯ НОВЫХ ИСТОЧНИКОВ ДАННЫХ, ПОПУЛЯЦИОННЫХ ИCСЛЕДОВАНИЙ И ПРЕДИКТИВНЫХ ТЕХНОЛОГИЙ
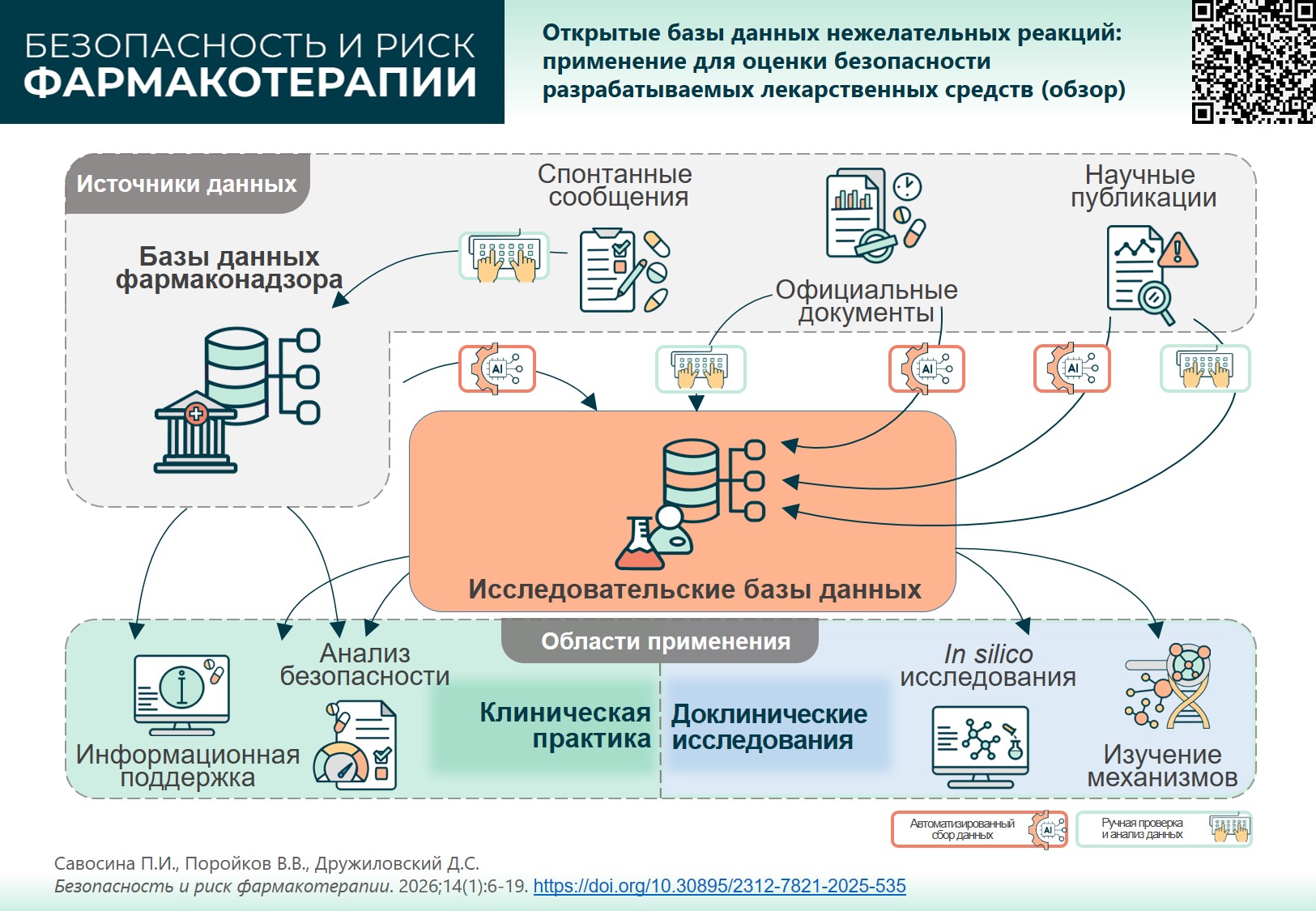
ВВЕДЕНИЕ. Важным этапом разработки лекарственных средств является оценка информации о безопасности уже зарегистрированных лекарственных препаратов (ЛП). Регуляторными органами и отдельными исследовательскими группами созданы и поддерживаются базы данных (БД) нежелательных реакций (НР) при применении ЛП. Сведения, агрегированные в таких БД, могут использоваться для создания справочных и обучающих наборов данных для экспериментальных и in silico исследований. Упростить выбор БД, релевантных для целей конкретного исследования, позволит предварительная оценка и систематизация представленной в них информации.
ЦЕЛЬ. Оценка возможности применения открытых баз данных для исследования безопасности лекарственных средств.
ОБСУЖДЕНИЕ. Изучены 11 БД с открытым доступом, содержащих сведения о НР ЛП: FAERS, DAEN, MedEffect Canada, EudraVigilance, VigiBase, SIDER, MetaADEDB, ADReCS-Target, T-ARDIS, OnSIDES, WWAD. Различия БД обусловлены прежде всего используемыми источниками информации: спонтанные сообщения (FAERS, DAEN, MedEffect Canada, EudraVigilance, VigiBase), инструкции по медицинскому применению ЛП и официальные документы (SIDER, OnSIDES, WWAD), научные публикации (ADReCS-Target) и другие открытые веб-ресурсы (MetaADEDB, T-ARDIS). Все рассмотренные БД могут быть использованы для информационной поддержки и анализа профиля безопасности ЛП. При проведении доклинических исследований, в частности для создания используемых в in silico методах обучающих выборок, полезны SIDER, MetaADEDB, ADReCS-Target, OnSIDES и WWAD. Генерация гипотез о возможных механизмах возникновения НР, поиск новых направлений репозиционирования ЛП могут быть осуществлены с помощью ADReCS-Target, WWAD и T-ARDIS благодаря представленной в них дополнительной информации о фармацевтических субстанциях и молекулярных мишенях. Использование методов автоматизированного анализа текстов без тщательной последующей ручной проверки при построении БД, таких как ADReCS-Target, T-ARDIS, OnSIDES и MetaADEDB, ограничивает их применение для задач, требующих высокой степени достоверности анализируемой информации.
ВЫВОДЫ. Рассмотренные БД НР могут служить ценным инструментом для решения широкого круга медико-биологических задач. При выборе БД, релевантной для конкретного исследования, необходимо учитывать принципы, лежащие в основе ее создания, поскольку различия в источниках и методах аннотирования могут влиять на достоверность результатов.
ВВЕДЕНИЕ. Несогласованность оценки серьезности нежелательных реакций (НР) остается актуальной проблемой фармаконадзора, в частности в отношении широко применяемых в медицинской практике биоаналогов инсулина. Это особенно важно для НР, связанных с фармакологическими эффектами инсулинов (гипо- и гипергликемия) и аллергическими реакциями, которые нередко расцениваются как серьезные при отсутствии клинического контекста. Подобная несогласованность снижает аналитическую ценность данных, приводя к накоплению недостоверной информации о безопасности лекарственного препарата.
ЦЕЛЬ. Сравнить оценку серьезности НР препаратов инсулина (инсулин аспарт, инсулин лизпро, инсулин гларгин) репортерами и отделом фармаконадзора держателя регистрационного удостоверения, выявить пути повышения качества заполнения данных при спонтанном репортировании.
МАТЕРИАЛЫ И МЕТОДЫ. Проведено ретроспективное обсервационное исследование спонтанных сообщений о НР, полученных с момента регистрации лекарственных препаратов инсулин аспарт, инсулин лизпро и инсулин гларгин производства ООО «ГЕРОФАРМ» в Российской Федерации (2021–2024 гг.). В выборку включены валидные случаи развития НР, кодированные по MedDRA v.25.1. Для оценки использовали критерии серьезности, установленные руководством ICH E2A «Управление данными о клинической безопасности: определения и стандарты для ускоренной отчетности» и Правилами надлежащей практики фармаконадзора ЕАЭС. Применяли методы описательной статистики и сравнительный анализ по предпочтительным терминам MedDRA.
РЕЗУЛЬТАТЫ. Зафиксированы значительные расхождения оценки: совпадение результатов оценки серьезности НР наблюдали лишь в 41,3% случаев, несоответствия – в 58,7%. В 99,6% случаев репортеры считали НР серьезными, тогда как держатель регистрационного удостоверения оценивал их как несерьезные. Наиболее частыми спорными критериями серьезности были «значимое медицинское событие» – 71,1% всех разногласий и «угроза жизни» – 25,0%. Различия в оценке серьезности в основном касались НР, связанных с фармакологическими эффектами инсулинов и реакциями гиперчувствительности. Более чем в половине случаев спонтанные сообщения содержали информацию, недостаточную для проведения медицинской оценки.
ВЫВОДЫ. Выявленные значительные различия в оценке серьезности НР могут быть связаны с недостаточным качеством представленных данных, частым использованием субъективных критериев оценки («угроза жизни», «значимое клиническое событие») и сохраняющимся недоверием врачей к биоаналогичным лекарственным препаратам. Для повышения эффективности фармаконадзора необходимы образовательные программы и мероприятия, направленные на повышение качества репортирования о НР.
ВВЕДЕНИЕ. Социальные медиа (социальные сети, форумы, сайты отзывов) могут содержать важную информацию о нежелательных реакциях при применении лекарственных препаратов. Исследования русскоязычных социальных медиа как источника информации для фармаконадзора в Российской Федерации ранее не проводились.
ЦЕЛЬ. Оценить возможность использования российской социальной сети «ВКонтакте» как дополнительного источника сообщений о нежелательных реакциях на примере мониторинга упоминаний о применении метформина, азитромицина, метронидазола и клотримазола.
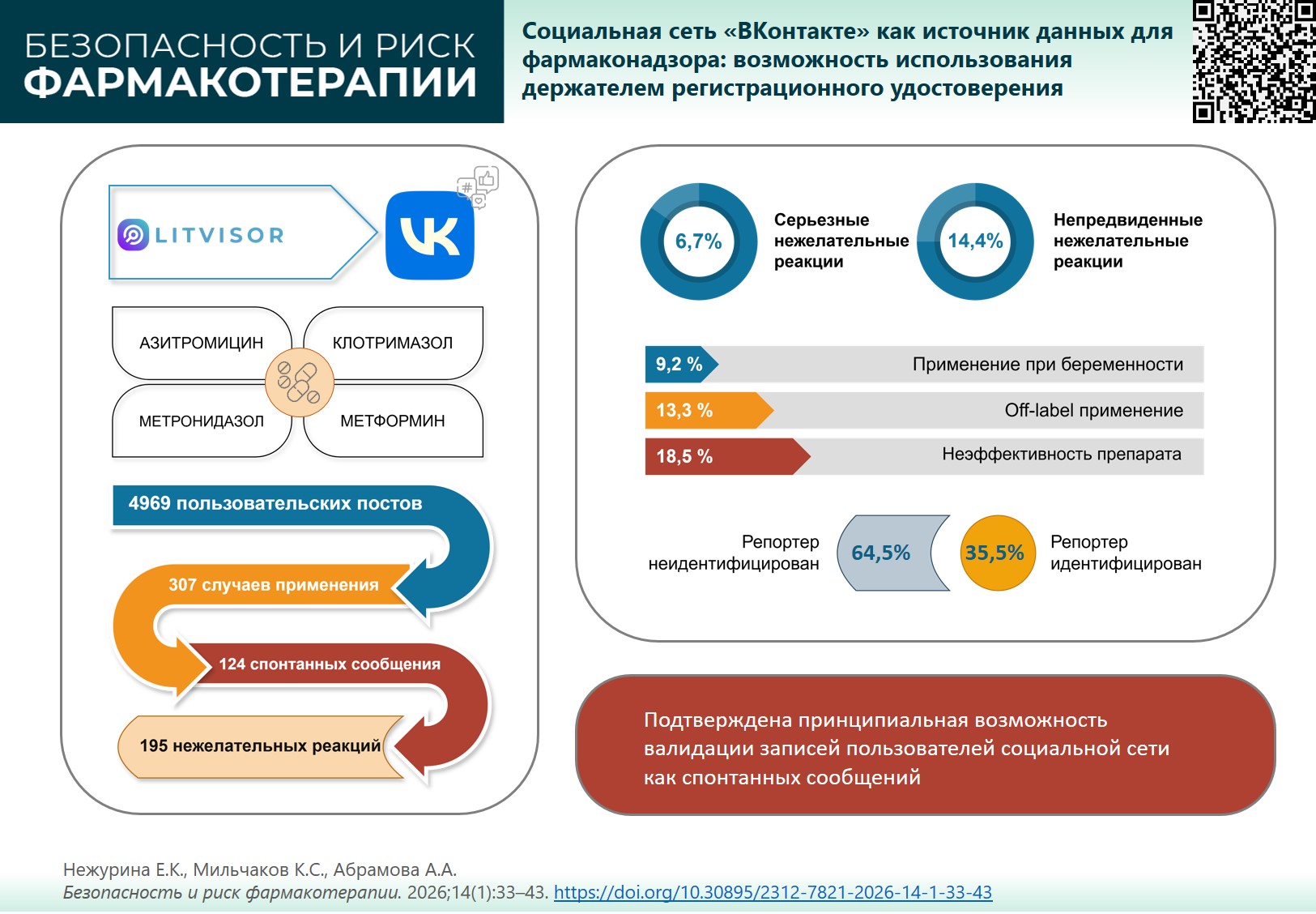
МАТЕРИАЛЫ И МЕТОДЫ. Проведен мониторинг социальной сети «ВКонтакте» в период с 01.09.2023 по 31.03.2024 при помощи программного обеспечения LITVISOR® для сбора пользовательских сообщений, содержащих упоминания о применении лекарственных препаратов с международными непатентованными наименованиями метформин, азитромицин, метронидазол, клотримазол. Оценивали полноту информации о репортере и пациенте в сообщениях, выявляли нежелательные реакции и особые ситуации по безопасности. Полученную информацию по безопасности кодировали в соответствии с терминологией MedDRA, оценивали серьезность и предвиденность нежелательных реакций.
РЕЗУЛЬТАТЫ. Мониторинг социальной сети «ВКонтакте» позволил обнаружить 4969 записей о случаях применения азитромицина, метформина, метронидазола и клотримазола. В 124 (2,5%) сообщениях выявлена информация о 195 нежелательных реакциях, которые были отнесены к 15 системно-органным классам. Как несерьезные были квалифицированы 93,3% случаев, как серьезные — 6,7%. Предвиденными были 85,6% нежелательных реакций, непредвиденными — 14,4%. Выявлены случаи off-label применения лекарственных препаратов, передозировки, применения у беременных женщин. В 35,5% спонтанных сообщений репортер был идентифицирован, в 89,5% был известен пол пациента, в 36,3% — возраст пациента.
ВЫВОДЫ. В исследовании показано, что мониторинг русскоязычной социальной сети «ВКонтакте» перспективен для получения данных по безопасности лекарственных препаратов, разрешенных к применению в Российской Федерации. Подтверждена принципиальная возможность валидации записей пользователей социальной сети как спонтанных сообщений.
ВВЕДЕНИЕ. Фармаконадзор обеспечивает безопасность препаратов благодаря постоянному мониторингу, и все же осведомленность фармацевтических работников остается недостаточной. Широко применяемый антацид ранитидин был изъят из обращения во всем мире в 2020 г. из-за примеси N-нитрозодиметиламина (НДМА), потенциального канцерогена. Несмотря на официальное изъятие ранитидина из обращения, сохраняется вероятность его необоснованного применения в практике. В этих условиях актуальной задачей становится оценка уровня профессиональной осведомленности фармацевтических работников.
ЦЕЛЬ. Выявление проблем системы фармаконадзора аптечных организаций Ливии и направлений ее совершенствования на примере оценки осведомленности работников аптек о безопасности ранитидина и причинах его изъятия из обращения.
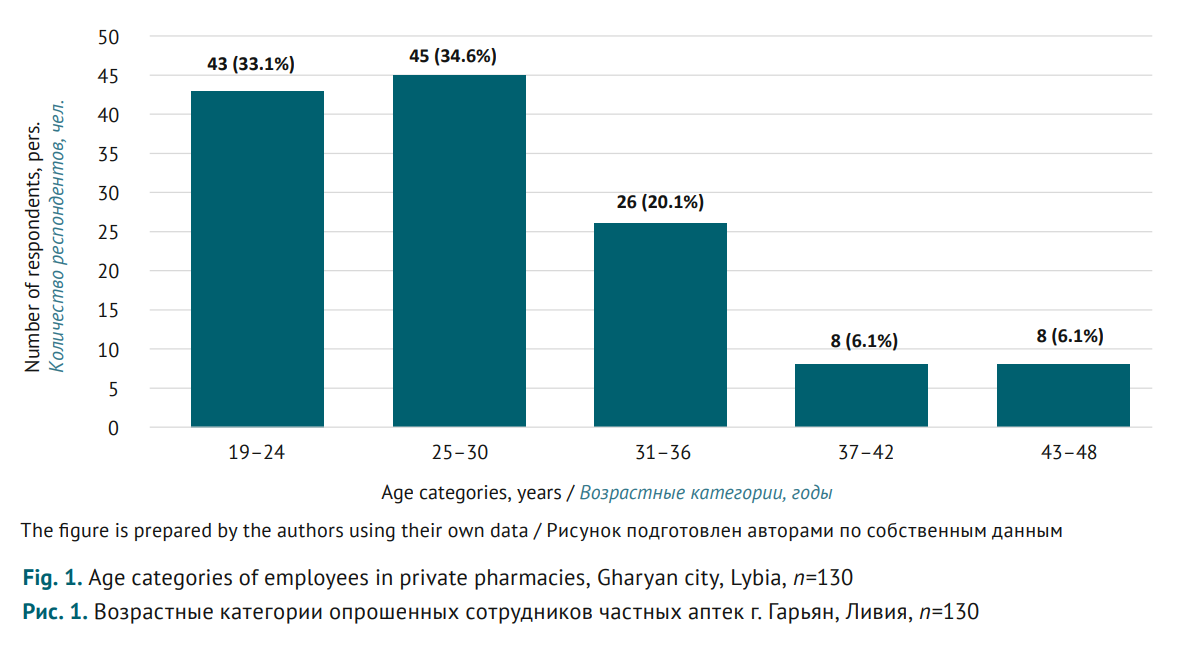
МАТЕРИАЛЫ И МЕТОДЫ. Поперечное исследование проводили с января по март 2023 г. среди 130 сотрудников аптек г. Гарьян (Ливия). Использовали структурированный опросник, имеющий три раздела: 1) демографические данные (возраст, пол, специализация, стаж); 2) базовые знания о фармаконадзоре (6 вопросов с ответами «Да/Нет»); 3) осведомленность об изъятии ранитидина из обращения (6 вопросов «Да/Нет»). Данные анализировали с помощью описательной статистики.
РЕЗУЛЬТАТЫ. Результаты проведенного опроса показали, что почти треть участников (36,2%) не знакомы с термином «фармаконадзор», более двух третей (63,8%) не знали о существовании Центра фармаконадзора в Ливии. Это противоречит ответам респондентов о фармаконадзорных мероприятиях: 78,5% указали, что проходили обучение по фармаконадзору, 81,5% знали о специальных бланках отчетности, которые нужно заполнять при выявлении побочного действия лекарственных препаратов, а 16,2% ранее готовили такие отчеты. О случаях отзыва лекарственных препаратов из-за связанных с ними рисков были осведомлены 55,4% участников. В то же время 79,2% респондентов указали, что ранитидин можно приобрести в аптеке, 30,8% неверно относили ранитидин, блокатор Н2-гистаминовых рецепторов, к антигистаминным препаратам. Источником канцерогенных примесей в препарате 61,5% респондентов считали загрязнения при производстве, и только 36,1% ответили, что примеси также могут образоваться вследствие неправильного хранения.
ВЫВОДЫ. Выявленные критические пробелы в знаниях о системе фармаконадзора и безопасности ранитидина обусловливают необходимость целенаправленного обучения сотрудников ливийских аптек и более активного законодательного урегулирования процедуры изъятия лекарственных препаратов из обращения.
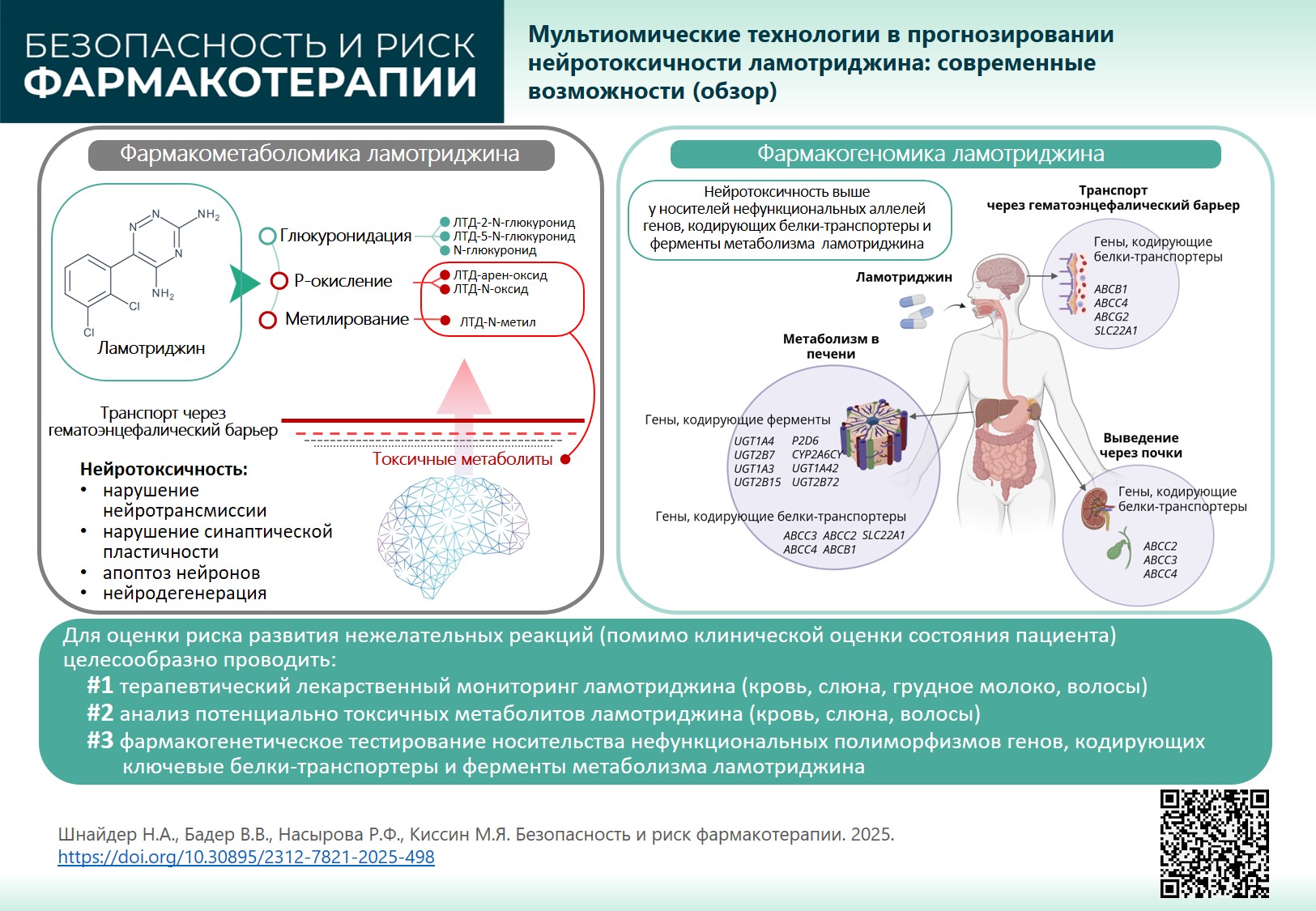
ВВЕДЕНИЕ. Ламотриджин (ЛТД) — один из наиболее часто назначаемых противоэпилептических препаратов второго поколения. Препарат имеет низкий тератогенный потенциал, однако обладает генетически и метаболически детерминированными нейротоксическим, гепатотоксическим, дерматотоксическим эффектами и в некоторых случаях может вызвать полиорганную недостаточность. Понимание механизмов действия ЛТД с учетом фармакогеномики и фармакометаболомики, определяющих особенности его метаболизма, транспорта и элиминации у конкретного пациента позволит обеспечить индивидуализацию терапии и повысить ее безопасность.
ЦЕЛЬ. Разработка подхода к терапии ламотриджином эпилепсии и других неврологических и психических заболеваний с учетом фармакогеномики и фармакометаболомики для снижения риска нейротоксичности препарата.
ОБСУЖДЕНИЕ. Метаболизм ЛТД осуществляется в печени глюкуронидацией (основной путь) и Р-окислением (второстепенный путь). В результате образуются как нейтральные, так и токсические (реактивные) метаболиты ЛТД, которые могут длительно циркулировать в крови, проникать через поврежденный гематоэнцефалический барьер у пациентов с терапевтически резистентными эпилептическими приступами и оказывать нейротоксический эффект, запуская или поддерживая механизмы нейродегенерации: нарушение нейротрансмиссии, синаптической пластичности, апоптоз нейронов. Большое значение в нейротоксичности ЛТД играют транспортные белки, участвующие в эффлюксе (выведении) токсических метаболитов из головного мозга в системный кровоток, а также из гепатоцитов в желудочно-кишечный тракт с желчью и через почки с мочой. Генетически детерминированное замедление эффлюкса препарата через гематоэнцефалический барьер (фармакогеномика) повышает нейротоксический потенциал ЛТД.
ВЫВОДЫ. Для оценки риска ЛТД-индуцированных нежелательных реакций наряду с клинической оценкой состояния пациента целесообразно проводить: 1) терапевтический лекарственный мониторинг (кровь, волосы, слюна, грудное молоко); 2) анализ потенциально токсичных метаболитов (кровь, слюна, волосы); 3) фармакогенетическое тестирование носительства нефункциональных полиморфизмов генов, кодирующих ключевые белки-транспортеры и ферменты, участвующие в метаболизме ЛТД. Внедрение результатов фармакогенетического и фармакометаболического тестирования в клиническую практику эпилептолога позволит снизить риск нейротоксичности ЛТД.
ВВЕДЕНИЕ. Рак молочной железы (РМЖ) занимает второе место в структуре смертности среди женского населения. Трижды негативный РМЖ считается одним из наиболее агрессивных по течению и трудно поддающимся терапии молекулярно-биологическим подтипом заболевания. Терапия метастатической формы трижды негативного РМЖ представляет собой актуальную проблему ввиду влияния многих факторов на эффективность лечения. Анализ и оценка нежелательных реакций химиотерапии пациентов являются ключевыми элементами обеспечения качества лекарственной помощи.
ЦЕЛЬ. Оценка рисков возникновения нежелательных реакций и тяжести их последствий при химиотерапии метастатической формы трижды негативного рака молочной железы для обоснования стратегий управления и предупреждения данных нежелательных реакций.
МАТЕРИАЛЫ И МЕТОДЫ. Использованы: метод контент-анализа научных публикаций, нормативных актов, национальных стандартов медицинской помощи взрослым при РМЖ, клинических рекомендаций терапии РМЖ взрослым; ретроспективный анализ первичной медицинской документации пациентов с метастатической формой трижды негативного рака молочной железы, проходивших лечение в Государственном бюджетном учреждении здравоохранения Астраханской области «Областной клинический онкологический диспансер» за 2023–2024 гг.
РЕЗУЛЬТАТЫ. Установлены терапевтические стратегии первой (доксорубицин + циклофосфамид, доцетаксел) и второй (паклитаксел + карбоплатин, эрибулин) линий лекарственной терапии метастатической формы трижды негативного РМЖ. Выявлены нежелательные реакции, возникающие при их назначении: фебрильная нейтропения, кардиотоксичность, периферическая нейропатия, лекарственная устойчивость, тошнота и рвота. В категорию наиболее высокого риска для двух линий терапии был отнесен риск развития фебрильной нейтропении, наиболее низкого — проявление тошноты и рвоты.
ВЫВОДЫ. Частота развития и профиль нежелательных реакций существенно варьируют в зависимости от применяемых схем и линий химиотерапии пациентов с метастатической формой трижды негативного РМЖ. При доминировании проявлений гематологической токсичности при назначении каждого из режимов стратегия «антрациклин — циклофосфамид» относится к повышенной категории риска возникновения нежелательных реакций. Наиболее безопасными для пациентов являются монорежимы эрибулина и доцетаксела. Результаты исследования могут быть основой для усовершенствования и оптимизации лекарственной терапии метастатической формы трижды негативного РМЖ.
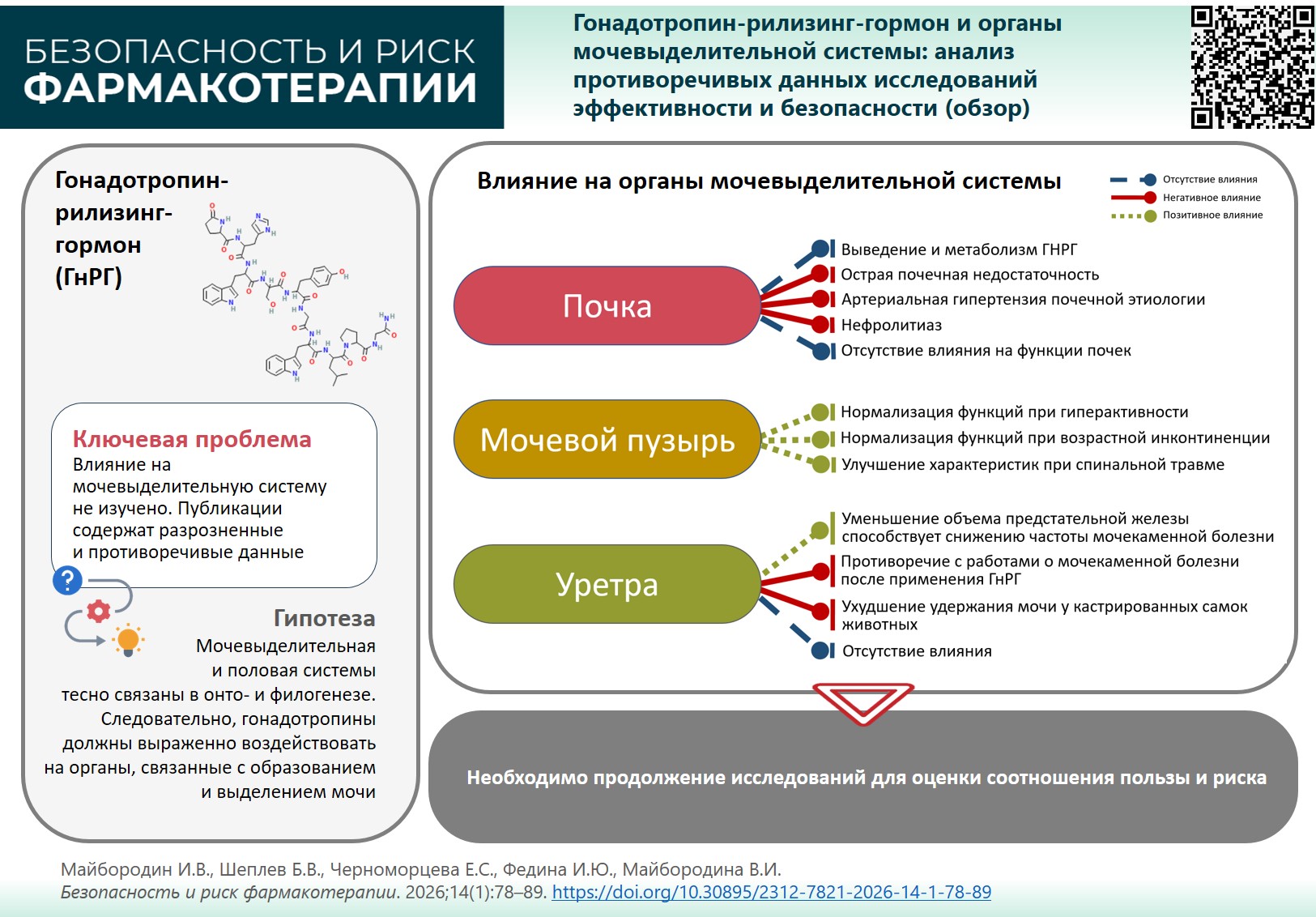
ВВЕДЕНИЕ. Препараты гонадотропин-рилизинг-гормона (ГнРГ) применяют при заболеваниях органов репродукции, как женских (вызывают временную медикаментозную менопаузу), так и мужских (с целью супрессии функций при доброкачественных и злокачественных заболеваниях). Половая и мочевыделительная системы тесно связаны в онто- и филогенезе. Обобщение и критический анализ имеющихся данных о влиянии препаратов ГнРГ на органы мочевыделительной системы позволит оценить имеющуюся информацию и определить направления дальнейших исследований.
ЦЕЛЬ. Систематизация имеющихся данных о пользе и рисках терапии ГнРГ в отношении мочевыделительной системы для планирования дальнейших исследований и разработки стратегий терапии.
ОБСУЖДЕНИЕ. Анализ результатов доклинических и клинических исследований показал, что ГнРГ и его метаболиты выводятся из организма преимущественно через почки. Препараты ГнРГ негативно влияют на функции и структуру почек: возможно развитие нефролитиаза вследствие нарушений кальциевого обмена, описаны случаи острого поражения почек вплоть до острой недостаточности. Структуры мочевого пузыря содержат рецепторы ГнРГ, что определяет высокий уровень связывания ГнРГ с его клетками. Высокие уровни ГнРГ и рецепторов ГнРГ при раке мочевого пузыря ассоциированы с повышением общей выживаемости у мужчин и ее снижением у женщин. Высокая экспрессия рецепторов ГнРГ на клеточных элементах рака определяет успешность применения препаратов ГнРГ для терапии новообразований мочевого пузыря. Аналоги ГнРГ оказывают положительный клинический эффект у женщин с возрастной менопаузальной инконтиненцией, непосредственно влияя на ткани мочевого пузыря, в том числе его сфинктерную систему, и уретру. Однако данные в некоторых рассмотренных статьях недостаточно обоснованы и статистически не подтверждены. В ряде работ сообщалось об отсутствии влияния препаратов ГнРГ на функции почек, уретры, а также на исходы опухолей мочевого пузыря.
ВЫВОДЫ. Явная недостаточность данных и противоречивость публикаций по каждому из аспектов действия ГнРГ на органы мочевыделительной системы свидетельствует о малой изученности этого вопроса. Необходимо продолжение прикладных и фундаментальных исследований влияния ГнРГ на мочевыводящие пути для оценки соотношения пользы и риска, создания новых, менее токсичных противораковых средств, эффективной профилактики и коррекции нежелательных реакций при гормонотерапии различных заболеваний.
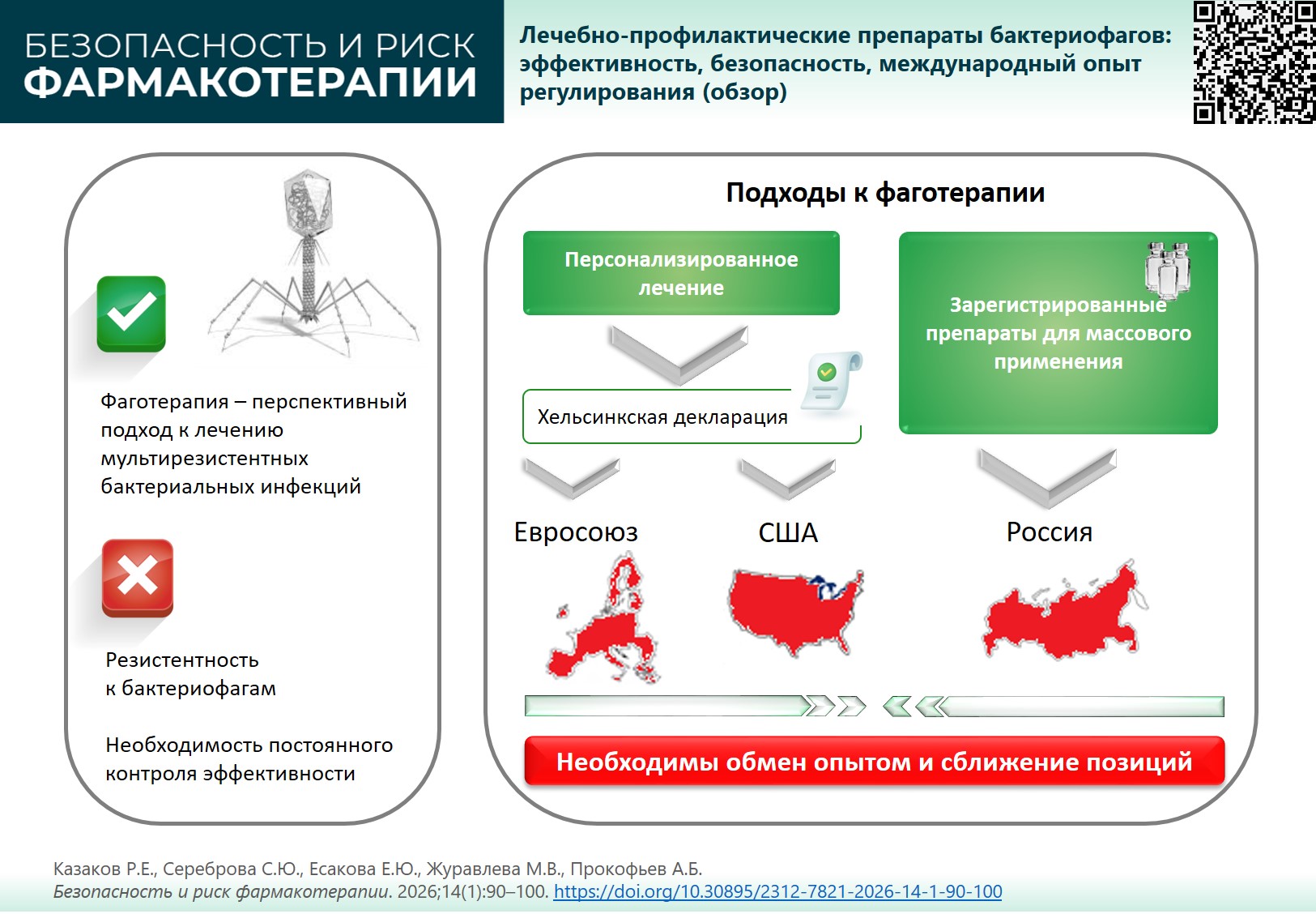
ВВЕДЕНИЕ. Препараты бактериофагов эффективны при бактериальных инфекциях, в том числе вызванных возбудителями с множественной лекарственной устойчивостью. Для разработки и широкого использования стандартизованных и персонализированных препаратов для фаготерапии необходима актуализация нормативных правовых и методических документов, регламентирующих разработку, проведение клинических исследований, регистрацию и обращение препаратов бактериофагов.
ЦЕЛЬ. Анализ мировых тенденций в области разработки, регистрации, оценки эффективности и безопасности препаратов бактериофагов для определения перспективных направлений развития фаготерапии в Российской Федерации.
ОБСУЖДЕНИЕ. Несмотря на доказанную эффективность бактериофагов, их широкое внедрение в клиническую практику затрудняют быстрое развитие резистентности у возбудителей инфекций, сложности доставки к очагу инфекции, а также недостаточная изученность безопасности фаготерапии. При снижении эффективности стандартизованных препаратов бактериофагов может потребоваться изменение рецептуры для актуализации штаммов, однако регуляторные механизмы для этого отсутствуют. В Российской Федерации зарегистрированы и применяются 14 стандартизованных препаратов бактериофагов, проведены их клинические исследования. В меньшей степени развито персонализированное применение бактериофагов. В США и государствах – членах Европейского союза, предъявляющих строгие требования к доказательствам безопасности и эффективности лекарственной терапии, фаготерапия не является официальным методом лечения и применяется лишь в отдельных случаях. В некоторых европейских странах, в частности, в Польше и Бельгии, фаготерапии уделяется большое внимание, но применение бактериофагов остается индивидуальным. В 2025 г. в Европейском союзе подготовлена рабочая версия концептуального документа по разработке и производству препаратов на основе бактериофагов для применения у человека. Но до сих пор ни один препарат для фаговой терапии не получил одобрения в соответствии с законодательствами Европейского союза и США.
ВЫВОДЫ. Россия имеет уникальный опыт применения стандартизованных фаговых препаратов. При этом регуляторные механизмы внесения изменений в состав уже зарегистрированных препаратов бактериофагов не разработаны ни в России, ни в других странах. Для глобального развития направления необходима международная гармонизация нормативной базы с учетом новых инициатив Европейского союза и США по созданию регуляторных документов, а также интенсификация исследований по преодолению резистентности бактерий к бактериофагам и изучение их долгосрочной безопасности.
ВВЕДЕНИЕ. Ласмидитан — новый селективный агонист серотониновых рецепторов 5-HT1F, одобренный Управлением по контролю за качеством продуктов питания и лекарственных средств США (FDA) в 2019 г. Купирует приступы мигрени за счет нейронального ингибирования, действует в центральной и периферической нервной системе. В отличие от триптанов (агонистов 5-HT1B/1D рецепторов), основной группы препаратов для купирования тяжелых приступов мигрени, ласмидитан не оказывает сосудосуживающего действия.
ЦЕЛЬ. Оценка места в лечении мигрени представителя нового класса противомигренозных препаратов (дитанов) ласмидитана на основании обзора особенностей механизма действия и данных по эффективности и безопасности.
ОБСУЖДЕНИЕ. Механизм действия ласмидитана при мигрени опосредован селективным воздействием на серотониновые рецепторы 5-HT1F на тригемино-васкулярном у ровне и в модулирующих путях болевой сигнализации в центральной нервной системе. Эффективность ласмидитана по сравнению с плацебо была достоверно продемонстрирована в трех рандомизированных клинических исследованиях (SAMURAI, SPARTAN, CENTURION, n=5910). В группе, включавшей пациентов с ишемической болезнью сердца, прекращение боли отмечалось у 31,4% пациентов (100 мг) и 38,8% (200 мг) vs 21,3% при приеме плацебо, исчезновение самого неприятного симптома — у 44,2% (100 мг) и 48,7% (200 мг) vs 33,5% для плацебо. Стабильность эффекта сохранялась у 13,6% (100 мг) и 17,3% (200 мг) пациентов. Нежелательные явления имели центральный и дозозависимый характер: головокружение (14,7%), парестезии (5,7%), сонливость (5,5%), усталость (3,8%), тошнота (3,4%), мышечная слабость (1,3%), гипоэстезия (1,2%); осложнения со стороны сердечно-сосудистой системы, в том числе у пациентов с ишемической болезнью сердца, не зарегистрированы. Большинство нежелательных явлений были легкими / умеренно выраженными, при длительном приеме ласмидитана частота их возникновения снижалась. Отмечены редкие случаи серотонинового синдрома в клинических исследованиях и при пострегистрационном применении. Также в течение 8 ч после приема ласмидитана снижается концентрация внимания и скорость реакции.
ВЫВОДЫ. Ласмидитан может рассматриваться в качестве альтернативы триптанам у пациентов с высоким сердечно-сосудистым риском либо при недостаточной эффективности триптанов. Следует оценивать возможность развития нежелательных явлений со стороны центральной нервной системы, учитывать вероятность нейропсихических осложнений, сопутствующую терапию и особенности профессиональной деятельности.
ВВЕДЕНИЕ. Хроническая обструктивная болезнь легких (ХОБЛ) — одна из ведущих причин смертности и значительных экономических потерь для системы здравоохранения. В Европе наблюдается тенденция к снижению заболеваемости, тогда как в России в 2022–2023 гг. она возросла на 5%, а экономическое бремя увеличилось с 0,20 до 0,34% ВВП. Для поиска путей снижения финансовой нагрузки на систему здравоохранения Российской Федерации необходим сравнительный анализ лучших международных и российских практик.
ЦЕЛЬ. Выявление и экономическое обоснование наиболее эффективных направлений для снижения финансовой нагрузки при ведении пациентов с ХОБЛ в Российской Федерации.
ОБСУЖДЕНИЕ. Выявлены ключевые различия между Российской Федерацией и странами Европейского союза в эпидемиологии и структуре затрат на ХОБЛ. В Европе (2001–2019 гг.) заболеваемость снизилась среди мужчин (–9,7%), но выросла среди женщин (+4,3%) в связи с увеличением распространенности табакокурения. В России заболеваемость продолжает расти (+5%), а смертность остается высокой (26% в общей структуре). В европейских странах основные прямые затраты приходятся на госпитализацию (35–64%) и лекарственную терапию (~25%), а доля косвенных расходов достигает 61–83%. В России структура затрат иная: доля косвенных затрат составляет 92,6%, и среди прямых затрат 76,1% приходится на лекарственное обеспечение и лишь 18,7% — на стационарное лечение. Эффективными мерами по снижению экономического бремени ХОБЛ являются: отказ от курения (снижает риск обострений на 39,7%; отношение рисков (HR) 0,65 при воздержании >10 лет), вакцинопрофилактика (снижает количество госпитализаций на 50%, а отказ от нее увеличивает уровень летальности в 162 раза), современная фармакотерапия (тройная терапия (антихолинергические препараты длительного действия + β2-агонисты длительного действия + ингаляционные глюкокортикостероиды) снижает частоту обострений на 24% и смертность на 49%) и легочная реабилитация (отношение шансов (OR) повторных госпитализаций 0,44), охват которой в России крайне низок (~10%).
ВЫВОДЫ. Для снижения экономического бремени ХОБЛ в Российской Федерации необходимо расширить охват профилактическими мероприятиями (антитабачные программы, вакцинация), развивать программы легочной реабилитации с использованием цифровых технологий, внедрять современные схемы фармакотерапии и повышать квалификацию врачей через систему непрерывного медицинского образования.
Объявления
2026-04-01
Cochrane: новая концепция синтеза доказательств в условиях меняющегося мира
На сайте Кокрейновского сотрудничества, информационным партнером которого является журнал «Безопасность и риск фармакотерапии», опубликована новая концепция синтеза доказательств в условиях меняющегося мира
| Еще объявления... |
ISSN 2619-1164 (Online)